
| A.由H2、I2、HI组成的平衡体系加压后颜色变深 |
| B.黄绿色的氯水光照后颜色变浅 |
| C.使用催化剂可加快SO2转化为SO3的速率 |
| D.将木炭粉碎后与O2反应,速率更快 |
科目:高中化学 来源:不详 题型:填空题
 cC(g)表示]化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):
cC(g)表示]化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):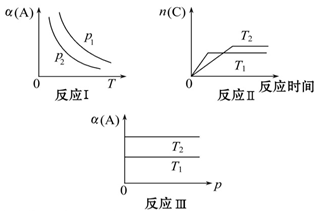
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 N2O4(g)△H=-57.2kJ·mol-1
N2O4(g)△H=-57.2kJ·mol-1
 大于”、“小”或“等于”)
大于”、“小”或“等于”)| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n 4 |
| n(N2O4)/mol | 0.00 | 0.05 | n 2 | 0.08 | 0.08 |
 不变,下列既能加快正反应速率又能提高NO2转化率的措施是
不变,下列既能加快正反应速率又能提高NO2转化率的措施是查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应:
醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应: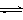 CH3OH(g)+H2O(g);△H=-49.0kJ/mol
CH3OH(g)+H2O(g);△H=-49.0kJ/mol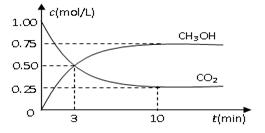
 _____;
_____; (精确到小数点后两位)。若提高温度到800oC进行达平衡时;K值__________,n(CH3OH)/n(CO2)比值__________(以上两空填“增大”、“减小”或“不变”);
(精确到小数点后两位)。若提高温度到800oC进行达平衡时;K值__________,n(CH3OH)/n(CO2)比值__________(以上两空填“增大”、“减小”或“不变”);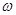 为__________;
为__________;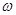 。则a、b、c的关系为__________。
。则a、b、c的关系为__________。 _____________________。
_____________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )| A.用X 表示的化学反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若升高温度Y的转化率减小,则正反应为吸热反应 |
| D.达到平衡时,Y与Z 的浓度相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )
pC(g)+ Q在密闭容器中进行,图中表示在不同反应时间t时,温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析下列判断正确的( )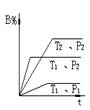
| A.T1 < T2 P1 > P2 m + n >p Q < 0 |
| B.T1 > T2 P1 < P2 m + n >p Q < 0 |
| C.T1 < T2 P1 > P2 m + n <p Q > 0 |
| D.T1 > T2 P1 < P2 m + n <p Q < 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Z反应影响的示意图,下列叙述正确的是
Z反应影响的示意图,下列叙述正确的是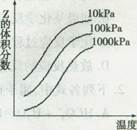
| A.X和Y中只有一种为气态,z为气态 |
| B.X、Y、Z均为气态 |
| C.上述可逆反应的正反应为放热反应 |
| D.上述反应的逆反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
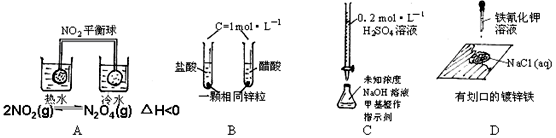
| 序号 | 实验现象 | 结 论 |
| A | 热水中平衡球颜色比冷水中深 | 升温,化学平衡向吸热反应方向移动 |
| B | 起始时产生气泡速率HCl > CH3COOH | 醋酸是弱电解质 |
| C | 溶液颜色由黄变橙,且30秒内不变色 | 已达滴定终点 |
| D | 划口处有蓝色沉淀 | 铁发生了析氢腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com