
【题目】草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,175℃时分解。
Ⅰ.用硝酸氧化法制备草酸晶体并测定其纯度,制备装置如图所示(加热、固定等装置略去)。
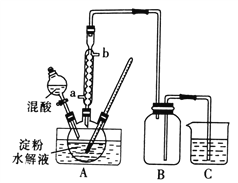
实验步骤如下
①糖化:先将淀粉水解为葡萄糖;
②氧化:在淀粉水解液中加入混酸(质量之比为3:2的65%HNO3与98%HSO4的混合物),在55~60℃下水浴加热发生反应;
③结晶、蒸发、干燥:反应后溶液经冷却、减压过滤,即得草酸晶体粗产品。
(1)装混酸的仪器名称为________;步骤②中,水浴加热的优点为__________。
(2)“②氧化”时发生的主要反应如下,完成下列化学方程式:
___C6H12O6+___HNO3 ![]() ___H2C2O4+9NO2↑+3NO↑+ ______
___H2C2O4+9NO2↑+3NO↑+ ______
(3)称取mg草酸晶体粗产品,配成100mL溶液。取20.00mL于锥形瓶中,用amoL·L-1KMnO4标准液标定,只发生
5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O反应,消耗KMnO4标准液体积为VmL,则所得草酸晶体(H2C2O4·2H2O)的纯度为___________。
Ⅱ.证明草酸晶体分解得到的产物
(4)甲同学选择下述装置验证产物CO2,装置B的主要作用是__________。
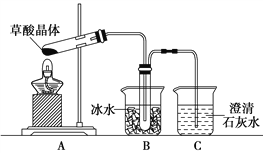
(5)乙同学认为草酸晶体分解的产物中除了CO2、H2O应该还有CO,为进行验证,选用甲同学实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验。
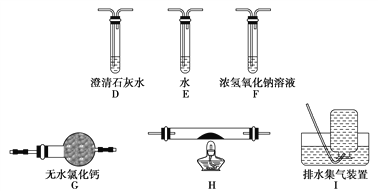
①乙同学的实验装置中,依次连接的合理顺序为A、B、_____________。其中装置H反应管中盛有的物质是________________________。
②能证明草酸晶体分解产物中有CO的现象是_____________________。
【答案】 分液漏斗 使受热均匀,便于控制温度 1C6H12O6+12HNO3 ![]() 3H2C2O4+9NO2↑+3NO↑+9_ H2O 12.6aV/8mⅹ100% 使升华的草酸冷凝,避免对CO2检验的干扰 FDGHDI CuO H中黑色固体变红色,第一个D装置无现象,第二个D装置出现白色浑浊,即可证明
3H2C2O4+9NO2↑+3NO↑+9_ H2O 12.6aV/8mⅹ100% 使升华的草酸冷凝,避免对CO2检验的干扰 FDGHDI CuO H中黑色固体变红色,第一个D装置无现象,第二个D装置出现白色浑浊,即可证明
【解析】分析:Ⅰ.(1)仪器识别;水浴加热的优点;(2)缺项配平;(3)根据反应关系计算纯度;
Ⅱ. (4)冰水混合物能够起到降温的作用;(5)草酸晶体分解生成三种氧化物,分别是水、二氧化碳和一氧化碳,加热条件下,氧化铜和一氧化碳反应生成铜和二氧化碳,以此解题。
详解: Ⅰ. (1) 装混酸的仪器名称为分液漏斗;水浴加热的优点是使受热均匀,便于控制温度。
根据得失电子守恒配平,根据原子守恒确定缺项为H2O,配平后得到1C6H12O6+12HNO3 ![]() 3H2C2O4+9NO2↑+3NO↑+9_ H2O 。
3H2C2O4+9NO2↑+3NO↑+9_ H2O 。
根据关系式:5H2C2O4![]() 2MnO4-,n(H2C2O4)=
2MnO4-,n(H2C2O4)= ![]() n(MnO4-)==
n(MnO4-)==![]() ×aV×10-3mol,草酸粗晶体中含草酸晶体的质量=
×aV×10-3mol,草酸粗晶体中含草酸晶体的质量=![]() aV×10-3×
aV×10-3×![]() ×126g,草酸晶体(H2C2O4·2H2O)的纯度为=
×126g,草酸晶体(H2C2O4·2H2O)的纯度为=![]() ×100%。
×100%。
Ⅱ. (4)装置B的主要作用是使草酸气体降温液化,避免对二氧化碳检验产生干扰,故填:使升华的草酸冷凝,避免对CO2检验的干扰。
(5)①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G、H、D、I。检验CO可利用加热条件下,氧化铜和一氧化碳反应生成铜和二氧化碳,再检验CO2,所以装置H反应管中盛有的物质是CuO。故填:FDGHDI ;CuO ;
②能证明有CO的现象是H中黑色固体变红色,第一个D装置无现象,第二个D装置出现白色浑浊,即可证明。故填:H中黑色固体变红色,第一个D装置无现象,第二个D装置出现白色浑浊,即可证明。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A. 2 mol水的摩尔质量为36g/mol
B. 摩尔是用来衡量微观粒子多少的一种物理量
C. 阿伏加德罗常数约为6.02×1023mol-1
D. 1mol·L-1的Na2SO4溶液中,含Na+的个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】装置(1)为铁镍(Fe-Ni)可充电电池:Fe+Ni2O3+3H2O ![]() Fe(OH)2+2Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,电极Y附近溶液先变红。下列说法正确的是
Fe(OH)2+2Ni(OH)2;装置(Ⅱ)为电解示意图。当闭合开关K时,电极Y附近溶液先变红。下列说法正确的是

A. 闭合开关K时,电极X的电极反应式为2H++2e-===H2↑
B. 闭合开关K时,电极A的电极反应式为Ni2O3+2e-+2H++H2O===2Ni(OH)2
C. 给装置(I)充电时,电极B上参与反应的物质被氧化
D. 给装置(I)充电时,OH通过阴离子交换膜移向电极A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol·L-1四氯金酸( HAuCl4)溶液中滴加0.1mol·L-1NaOH溶液,滴定曲线如图1,含氯微粒的物质的量分数(δ)随pH变化关系如图2,则下列说法不正确的是
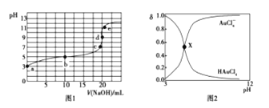
A. b点溶液中存在关系:2c(H+)+ c(HAuCl4)=2c(OH-)+ c(AuCl4-)
B. X点描述的是滴定曲线中b点含氯微粒的物质的量分数δ与pH的关系
C. c点溶液中存在关系:c(Na+)=c(AuCl4-)
D. d点时,溶液中微粒浓度的大小关系为c(Na+)>c(AuCl4-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是( )

A.a极是负极,该电极上发生氧化反应
B.b极反应是O2+4OH--4e-===2H2O
C.总反应方程式为2H2+O2===2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银锌电池是一种常见化学电源,这种银锌电池的续航能力要比锂离子电池强,有望取代锂电池。其放电过程可表示为Zn+Ag2O+H2O=Zn(OH)2+2Ag,其工作示意图如下。下列说法不正确的是 ( )

A. 放电过程中, 化学能转化为电能
B. 放电过程中, 阳离子移向Ag2O 电极
C. Zn 电极的电极反应式:Zn-2eˉ+2OHˉ=Zn(OH)2
D. 放电过程中电解质溶液的碱性不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A. 氢氟酸、氯水、AgNO3 溶液保存在棕色玻璃瓶中
B. 镁条可以在二氧化碳气体中燃烧
C. 二氧化硫能漂白某些物质,加热后可恢复原色
D. 常温下铁片遇浓硫酸会发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对科学家的相关成果的说法正确的是( )
A. 屠呦呦发现抗疟新药青蒿素(C15H22O5),青蒿素属于烃类
B. 闵恩泽研发重油裂解的催化剂,催化裂解可以获得很多重要的化工原料
C. 凯库勒研究了苯环的结构,苯环是碳碳单键和碳碳双键交替的结构
D. 门捷列夫提出元素周期律,元素周期律指元素的性质随相对原子质量的递增而呈周期性的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子反应方程式为( )
A. Ba(OH)2溶液中加入少量NaHCO3溶液:HCO3-+Ba2++OH-=BaCO3![]() +H2O
+H2O
B. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:3Ba2++3SO42-+2Al3++6OH-═2BaSO4↓+2Al(OH)3↓
C. NH4HCO3稀溶液与过量的KOH溶液反应:HCO3-+OH-=CO32-+H2O
D. 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com