
| △ |
| △ |


科目:高中化学 来源: 题型:
| A、某些馆的外壳使用非晶硅薄膜,以充分利用太阳能 |
| B、快餐盒用生物质材料“玉米塑料”(主要成分为可降解聚乳酸)做成 |
| C、使用的卫生纸都是再生纸 |
| D、把世博会期间产生的垃圾焚烧或深埋处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3P2表示3P能级有两个轨道 |
| B、同一原子中1S、2S、3S电子的能量逐渐降低 |
| C、氢原子电子云的一个小黑点表示一个电子 |
| D、处于最低能量的原子叫基态原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
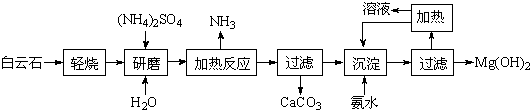
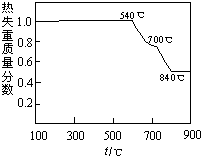
查看答案和解析>>
科目:高中化学 来源: 题型:
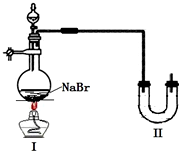 某学校同学进行乙醇的化学性质实验探究学习,以下为他们的学习过程.
某学校同学进行乙醇的化学性质实验探究学习,以下为他们的学习过程.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
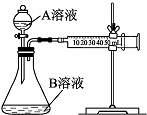 实验小组利用酸性KMnO4溶液与H2C2O4溶液反应研究影响反应速率的因素.
实验小组利用酸性KMnO4溶液与H2C2O4溶液反应研究影响反应速率的因素.查看答案和解析>>
科目:高中化学 来源: 题型:
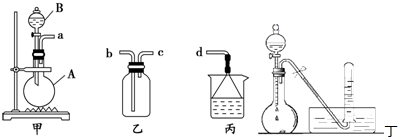
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象或预期试验先行 | 现象解释(用离子方程式表示) | ||
| 猜想② | (1) | 溶液PH=8 | --- | |
| 向PH=2的硫酸中滴加Na2S2O3溶液 | (2) | S2O
| ||
| 猜想③ | 向新制氯水(PH<2)中滴加少许Na2S2O3溶液 | 氯水颜色变浅 | (3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔质量:g?mol-1 |
| B、密度:g?mL-1 |
| C、气体摩尔体积:L |
| D、阿伏加德罗常数:mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com