
 ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó³ĘĪŖ»ī»Æ·Ö×Ó£¬Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ/mo1±ķŹ¾£®ĒėČĻÕę¹Ū²ģČēĶ¼£¬Č»ŗó»Ų“šĪŹĢā£ŗ
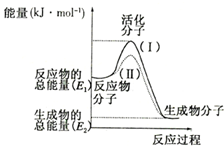
ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅæÉÄÜ·¢Éś»Æѧ·“Ó¦£¬ÕāŠ©·Ö×Ó³ĘĪŖ»ī»Æ·Ö×Ó£¬Ź¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ潊»ī»ÆÄÜ£¬Ę䵄Ī»Ķس£ÓĆkJ/mo1±ķŹ¾£®ĒėČĻÕę¹Ū²ģČēĶ¼£¬Č»ŗó»Ų“šĪŹĢā£ŗ·ÖĪö £Ø1£©ŅĄ¾ŻĶ¼Ļó·ÖĪö·“Ó¦ĪļµÄÄÜĮæ“óÓŚÉś³ÉĪļµÄÄÜĮ棬·“Ó¦·ÅČČ£»ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅÄÜ·¢Éś»Æѧ·“Ó¦£¬·“Ó¦ŠčŅŖÄÜĮ棻·“Ó¦µÄģŹ±ä=Éś³ÉĪļµÄÄÜĮæ-·“Ó¦ĪļµÄÄÜĮ棻
£Ø2£©Ķ¼Ź¾ĪļÖŹ·“Ó¦Ē°ŗóÄÜĮæ±ä»Æ£¬·“Ó¦ĪļÄÜĮæøßÓŚÉś³ÉĪļÄÜĮ棬·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬¾Ż“Ė·ÖĪöŃ”ĻīÖŠµÄ·“Ó¦ŹĒ·ÅČČ·“Ó¦µÄ·ūŗĻ£»
£Ø3£©·“Ó¦µÄ»ī»ÆÄÜŹĒŹ¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ棬ŅĄ¾ŻĶ¼ĻóÄÜĮæ¹ŲĻµæÉÖŖ£¬Äę·“Ó¦µÄ»ī»ÆÄÜ=Õż·“Ó¦µÄ»ī»ÆÄÜ+·“Ó¦µÄģŹ±ä£»
£Ø4£©“Ó“żĒó·“Ó¦³ö·¢·ÖĪö·“Ó¦Īļ”¢Éś³ÉĪļŌŚĖłøų·“Ó¦ÖŠµÄĪ»ÖĆ£¬ĶعżĻą»„¼Ó¼õæÉµĆ£¬¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł”Į2-¢ŚµĆµ½£®
½ā“š ½ā£ŗ£Ø1£©ŅĄ¾ŻĶ¼Ļó·ÖĪö·“Ó¦ĪļµÄÄÜĮæ“óÓŚÉś³ÉĪļµÄÄÜĮ棬·“Ó¦·ÅČČ£»ŌŚ»Æѧ·“Ó¦ÖŠ£¬Ö»ÓŠ¼«ÉŁŹżÄÜĮæ±ČĘ½¾łÄÜĮæøߵƶąµÄ·“Ó¦Īļ·Ö×Ó·¢ÉśÅöײŹ±²ÅÄÜ·¢Éś»Æѧ·“Ó¦£¬·“Ó¦ŠčŅŖÄÜĮ棻·“Ó¦µÄģŹ±ä=Éś³ÉĪļµÄÄÜĮæ-·“Ó¦ĪļµÄÄÜĮ棻”÷H=£ØE2-E1 £©KJ/mol£»
¹Ź“š°øĪŖ£ŗ·ÅČČ£»£ØE2-E1 £©KJ/mol£»
£Ø2£©Ķ¼Ź¾ĪļÖŹ·“Ó¦Ē°ŗóÄÜĮæ±ä»ÆĄń·žŅµĪńÄÜĮæøßÓŚÉś³ÉĪļ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬
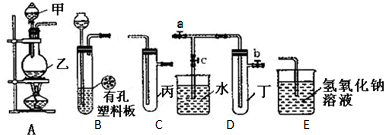
A£®Ė®ÕōĘųÓėĢæ·“Ó¦ŠčŅŖøßĪĀ½ųŠŠ£¬·“Ó¦ŹĒĪüČČ·“Ó¦£¬¹ŹA²»·ūŗĻ£»
B£®ÓĆĖ®Ļ”ŹĶĒāŃõ»ÆÄĘČÜŅŗ¹ż³ĢÖŠČÜŅŗĪĀ¶Č±ä»Æ²»“󣬲»ŹĒ»Æѧ·“Ó¦£¬¹ŹB²»·ūŗĻ£»
C£®ĀĮ·ŪÓėFe2O3·“Ó¦£¬Ņż·¢ŗó·“Ó¦¼ĢŠų½ųŠŠĪŖ·ÅČČ·“Ó¦£¬¹ŹC·ūŗĻ£»
D£®×ĘČȵÄĢ¼ÓėCO2·“Ó¦ŹōÓŚĪüČČ·“Ó¦£¬¹ŹD²»·ūŗĻ£»
¹Ź“š°øĪŖ£ŗC£»
£Ø3£©·“Ó¦µÄ»ī»ÆÄÜŹĒŹ¹ĘÕĶØ·Ö×Ó±ä³É»ī»Æ·Ö×ÓĖłŠčĢį¹©µÄ×īµĶĻŽ¶ČµÄÄÜĮ棬ŅĄ¾ŻĶ¼ĻóÄÜĮæ¹ŲĻµæÉÖŖ£¬Äę·“Ó¦µÄ»ī»ÆÄÜ=Õż·“Ó¦µÄ»ī»ÆÄÜ+·“Ó¦µÄģŹ±ä£»H2£Øg£©+$\frac{1}{2}$O2£Øg£©ØTH2O£Øg£©”÷H=-241.8kJ•mol-1£¬øĆ·“Ó¦µÄ»ī»ÆÄÜĪŖ167.2kJ•mol-1£¬ŌņĘäÄę·“Ó¦µÄ»ī»ÆÄÜ=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol£»
¹Ź“š°øĪŖ£ŗ409.0KJ/mol£»
£Ø4£©¢ŁCH4£Øg£©+H2O£Øg£©ØTCO£Øg£©+3H2£Øg£©”÷H=+206.2kmol-1
¢ŚCH4£Øg£©+CO2£Øg£©ØT2CO£Øg£©+2H2£Øg£©”÷H=+247.4kJmol-1
¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł”Į2-¢ŚµĆ£ŗCH4£Øg£©+2H2O£Øg£©ØTCO2£Øg£©+4H2£Øg£©”÷H=165.0kmol-1£¬
¹Ź“š°øĪŖ£ŗCH4£Øg£©+2H2O£Øg£©ØTCO2£Øg£©+4H2£Øg£©”÷H=+165.0kmol-1£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦µÄÄÜĮæ±ä»ÆÓė·“Ó¦µÄģŹ±ä¹ŲĻµµÄ·ÖĪöÅŠ¶Ļ”¢·“Ó¦»ī»ÆÄܵÄÅŠ¶Ļ¼ĘĖć”¢ČČ»Æѧ·½³ĢŹ½ŗĶøĒĖ¹¶ØĀɵļĘĖć”¢Ķ¼ĻóµÄ×ŪŗĻÓ¦ÓĆ£¬¶Į¶®Ķ¼Ļó£¬ģŹ±äŗĶ»ī»ÆÄܼĘĖć·½·ØµÄĄķ½āŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×±½ | B£® | ±ūĶé | C£® | 2-¼×»ł¶”Ķé | D£® | 2£¬2-¶ž¼×»ł±ūĶé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ¼ÓČėŹŌ¼Į | ¶ŌÓ¦»Æѧ»ņĄė×Ó·½³ĢŹ½ | ||
| A | ŅŅĶé£ØŅŅĻ©£© | ĒāĘų | CH2=CH2+H2$”ś_{¼ÓČČ}^{Ni}$CH3CH3 |
| B | CH3COOC2H5£ØCH3COOH£© | NaOHČÜŅŗ | CH3COOH+NaOH=CH3COONa+H2O |
| C | MgCl2£Ø FeCl3£© | °±Ė® | Fe3++3NH3•H2O=Fe£ØOH£©3”ż+3NH4+ |
| D | Fe2+£ØFe3+£© | Fe·Ū | 2Fe3++Fe=3Fe2+ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X”¢Y”¢Z”¢WµÄŌ×Ó°ė¾¶ŅĄ“Ī¼õŠ” | |
| B£® | WÓėXŠĪ³ÉµÄ»ÆŗĻĪļÖŠŅ»¶ØÖ»ŗ¬Ąė×Ó¼ü | |
| C£® | WµÄĒā»ÆĪļÓėĘä×īøßÕż¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļæÉŅŌĻą»„·“Ӧɜ³ÉŃĪ | |
| D£® | ČōWÓėYµÄŌ×ÓŠņŹżĻą²ī5£¬Ōņ¶žÕߊĪ³É»ÆŗĻĪļµÄ»ÆѧŹ½Ņ»¶ØĪŖY2W3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«æéדµÄCŃŠ³É·Ūĩד | |
| B£® | ½«ČŻĘ÷µÄĢå»żĖõŠ”Ņ»°ė | |
| C£® | ±£³ÖĢå»ż²»±ä£¬³äČėN2Ź¹ĢåĻµŃ¹ĒæŌö“ó | |
| D£® | ±£³ÖŃ¹Ēæ²»±ä£¬³äČėN2Ź¹ČŻĘ÷Ģå»ż±ä“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com