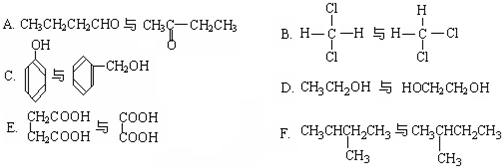
按要求完成下列问题:
(1)工业上通常把氯气通入石灰乳中来制漂白粉,该反应的化学方程式为______,还原剂是______.
(2)现有:①石灰水; ②水玻璃; ③氯化钡溶液.在上面四种溶液分别通入过量的CO2后,能产生白色浑浊有______(填序号);所发生反应离子方程式为:______.
(3)硫酸亚铁是一种可用于治疗缺铁性贫血的药剂,而硫酸铁则无这种药效.当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是______.如果药片已经失效,应如何检验?简述主要步骤:取少量研碎的药片放入烧杯中,加适量的水溶解,______;现象和结论______.
解:(1)工业上把氯气通入石灰乳中来制漂白粉,氯气和强碱氢氧化钙反应生成氯化钙、次氯酸钙和水,
即2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,该反应中化合价变化的元素是Cl,所以氯气是还原剂,
故答案为:2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;Cl2;
(2)氢氧化钙和过量的二氧化碳反应生成碳酸氢钙,硅酸钠和二氧化碳反应生成硅酸沉淀,氯化钡溶液和二氧化碳不发生反应,故答案为:②;SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-;
(3)亚铁离子具有较强的还原性,易被空气中的氧气氧化,所以当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是保护FeSO4不被空气中的氧气氧化成Fe2(SO4)3,三价铁离子检验所用的试剂是硫氰化钾,三价铁遇到硫氰酸钾会显示红色,而亚铁离子则不具备该性质,故答案为:保护FeSO4不被空气中的氧气氧化成Fe2(SO4)3;然后滴加几滴KSCN溶液;反应后溶液显血红色,则表明该药片已经失效.
分析:(1)工业上利用氯气和氢氧化钙的反应来制漂白粉,氯气和强碱反应生成盐酸盐、次氯酸盐和水,化合价升高元素所在的反应物是还原剂;
(2)根据物质的性质来回答;
(3)亚铁离子具有较强的还原性,易被空气中的氧气氧化,三价铁离子检验所用的试剂是硫氰化钾.
点评:本题考查学生亚铁离子和三价铁之间的性质,综合性较强,可以根据所学知识进行回答,难度较大.



 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
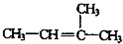 的名称是
的名称是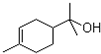 的分子式是
的分子式是