


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是国际单位制中的一个基本物理量 |
| B、萃取操作时,可以选择有机萃取剂,且萃取剂的密度必须比水大 |
| C、当光束分别通过氢氧化铁胶体、氯化铁溶液时,都可以从侧面看见光亮的通路 |
| D、根据分散质粒子的直径大小,分散系可分为溶液、胶体和浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuCO3 |
| B、Na2SO4 |
| C、CuSO4 |
| D、Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有一盛有常见固体物质M的试剂瓶,标签已破损(如图所示),请根据其性质回答下列问题:
现有一盛有常见固体物质M的试剂瓶,标签已破损(如图所示),请根据其性质回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关信息 | |
| X | X原子基态时最外层电子数是其内层电子数的2倍 |
| Y | Y原子基态时2p原子轨道上有3个未成对电子 |
| Z | Z的基态原子最外层电子排布式为:nsnnpn+2 |
| W | W的原子序数为24 |
查看答案和解析>>
科目:高中化学 来源: 题型:
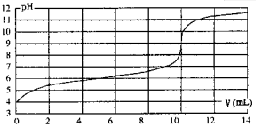
| A、HA的浓度为1×10-4mol?L-1 |
| B、实验时可选甲基橙作指示剂 |
| C、V=10mL,酸碱恰好中和 |
| D、pH=7时,溶液中c(Na+)>c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C原子采取sp杂化 |
| B、甲醛分子为三角锥形结构 |
| C、C原子采取sp3杂化 |
| D、甲醛分子为平面三角形结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
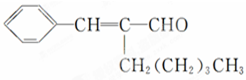
| A、在加热和催化剂作用下,能被氢气还原 |
| B、能被酸性高锰酸钾溶液氧化 |
| C、在一定条件下能与溴发生取代反应 |
| D、不能与氢溴酸发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com