
【题目】(1)在标准状况下,将充满NO2的试管倒扣到盛水的水槽中,一段时间后,试管内气体的体积是试管体积的________________,假设试管内溶质不扩散,则试管内溶液中溶质的物质的量浓度为___________________。
(2)某铁的“氧化物”样品,用5mol/L的盐酸100mL恰好完全溶解,所得溶液还能吸收标准状况下1.12L氯气,使其中Fe2+恰好全部转化为Fe3+,发生反应的离子方程式为_________,该样品中Fe和O的个数比为_______________。
(3)向盛有10mL1mol/LNH4Al(SO4)2溶液的烧杯中滴加1mol/LNaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:(已知NH4++OH-=NH3·H2O)
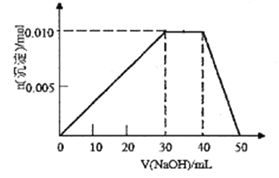
①写出滴加NaOH溶液40~50mL时反应的离子方程式:__________________。
②若10mL1mol/LNH4Al(SO4)2溶液中改加20mL1.15mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_________________mol。
【答案】 1/3 1/22.4mol/L或0.045mol/L 2Fe2++Cl2=2Fe3++2Cl- 4:5 Al(OH)3+OH-=AlO2-+2H2O 0.024
【解析】试题分析:(1)根据![]() 分析;根据
分析;根据![]() 计算试管内溶液中溶质的物质的量浓度;(2)Fe2+被氯气氧化为Fe3+,氯气被还有为Cl-;铁的“氧化物”中氧原子与盐酸中氢离子反应生成水,铁的“氧化物”中铁原子最终生成FeCl3,根据元素守恒计算Fe和O的个数比;(3)①滴加NaOH溶液40~50mL时沉淀溶解,是Al(OH)3与OH-反应生成AlO2- ;②10mL 1molL-1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42-的物质的量为0.02mol,20mL 1.15mol/L Ba(OH)2溶液中Ba2+物质的量为0.023mol,OH-为0.046mol,发生的反应有SO42-+Ba2+=BaSO4↓,根据图像可知OH-依次发生Al3++3OH-=Al(OH)3↓、 NH4++OH-=NH3H2O、 Al(OH)3+OH-=AlO2-+2H2O
计算试管内溶液中溶质的物质的量浓度;(2)Fe2+被氯气氧化为Fe3+,氯气被还有为Cl-;铁的“氧化物”中氧原子与盐酸中氢离子反应生成水,铁的“氧化物”中铁原子最终生成FeCl3,根据元素守恒计算Fe和O的个数比;(3)①滴加NaOH溶液40~50mL时沉淀溶解,是Al(OH)3与OH-反应生成AlO2- ;②10mL 1molL-1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42-的物质的量为0.02mol,20mL 1.15mol/L Ba(OH)2溶液中Ba2+物质的量为0.023mol,OH-为0.046mol,发生的反应有SO42-+Ba2+=BaSO4↓,根据图像可知OH-依次发生Al3++3OH-=Al(OH)3↓、 NH4++OH-=NH3H2O、 Al(OH)3+OH-=AlO2-+2H2O
解析:(1)根据![]() ,3体积的NO2与水反应后生成1体积的NO气体,所以试管内气体的体积是试管体积的
,3体积的NO2与水反应后生成1体积的NO气体,所以试管内气体的体积是试管体积的![]() ;设试管的体积是VL,则NO2的物质的量是
;设试管的体积是VL,则NO2的物质的量是![]() ,生成硝酸的物质的量是
,生成硝酸的物质的量是![]() ;试管中液体的体积是
;试管中液体的体积是![]() ,根据
,根据![]() ,试管内溶液中溶质的物质的量浓度是
,试管内溶液中溶质的物质的量浓度是 ;(2)Fe2+被氯气氧化为Fe3+,氯气被还有为Cl-,反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl-;铁的“氧化物”中氧原子与盐酸中氢离子反应生成水,氢离子的物质的量是5mol/L×0.1L=0.5mol,所以氧原子的物质的量是0.25mol;铁的“氧化物”中铁原子最终生成FeCl3,氯元素的物质的量是
;(2)Fe2+被氯气氧化为Fe3+,氯气被还有为Cl-,反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl-;铁的“氧化物”中氧原子与盐酸中氢离子反应生成水,氢离子的物质的量是5mol/L×0.1L=0.5mol,所以氧原子的物质的量是0.25mol;铁的“氧化物”中铁原子最终生成FeCl3,氯元素的物质的量是![]() ,所以铁原子的物质的量是0.2mol,根据元素守恒Fe和O的个数比0.2:0.25=4:5;(3)①滴加NaOH溶液40~50mL时沉淀溶解,是Al(OH)3与OH-反应生成AlO2- ,反应离子方程式是Al(OH)3+OH-=AlO2-+2H2O;②10mL 1molL-1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42-的物质的量为0.02mol,20mL 1.15 molL-1Ba(OH)2溶液中Ba2+物质的量为0.023mol,OH-为0.046mol,由SO42-+Ba2+=BaSO4↓,可知SO42-不足,故可以得到0.02mol BaSO4,
,所以铁原子的物质的量是0.2mol,根据元素守恒Fe和O的个数比0.2:0.25=4:5;(3)①滴加NaOH溶液40~50mL时沉淀溶解,是Al(OH)3与OH-反应生成AlO2- ,反应离子方程式是Al(OH)3+OH-=AlO2-+2H2O;②10mL 1molL-1 NH4Al(SO4)2溶液中Al3+ 物质的量为0.01mol,NH4+的物质的量为0.01mol,SO42-的物质的量为0.02mol,20mL 1.15 molL-1Ba(OH)2溶液中Ba2+物质的量为0.023mol,OH-为0.046mol,由SO42-+Ba2+=BaSO4↓,可知SO42-不足,故可以得到0.02mol BaSO4,

反应剩余OH-为0.046mol-0.03mol=0.016mol,![]()
反应剩余OH-为0.016mol-0.01mol=0.006mol,
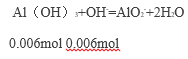
故得到Al(OH)3沉淀为0.01mol-0.006mol=0.004mol
则最终得到固体为0.02mol+0.004mol=0.024mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl﹣、SO42﹣中的几种离子.
a.取0.1mL该废水于管中,加入足量的Ba(N03)溶液和稀硝酸,产生白色沉淀,充分反应后过滤,向滤液中加入AgNO3溶液无沉淀产生.
b.另取10mL该废水于管中,滴加NaOH溶液先产生白色沉淀,后部分沉淀溶解.生成沉淀的物质的量随加入NaOH物质的量关系如图所示.
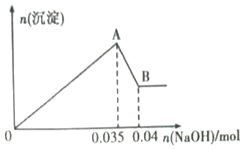
根据上述实验和图表数据:
(1)该废水中一定不含有的离子有______________(填离子符号).
(2)实验室配制100mL1molL﹣1的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要_____________(填仪器名称).
(3)写出A→B过程中发生反应的离子方程式:_________________________.
(4)该废水中,c(Al3+)=_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的每个方格表示有关的一种反应物或生成物,M分解生成A、B、C的物质的量之比为l:l:1,其中A和C为无色气体。
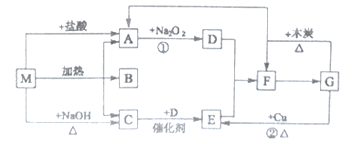
(1)物质M是__________(写名称),C是_____________(写化学式);
(2)M与盐酸反应生成A的离子方程式:_______________________________;
(3)反应②的离子方程式:_________________________________________________;
(4)G与木炭反应的化学方程式:_________________________________________;
(5)F生成G的化学方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:M(g)+N(g)P(g)+Q(g) H>0,请回答下列问题:
(1)在某温度下,反应物起始浓度分别为:c(M)=1molL﹣1 , c(N)=2.4molL﹣1 , 达到平衡后,M的转化率为60%,此时N的转化率为
(2)若反应温度升高,转化率(填“增大”、“减少”或“不变”).
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=4molL﹣1 , c(N)=a molL﹣1;达到平衡后,c(P)=2molL﹣1 , a= .
(4)若反应温度不变,反应物的起始浓度分别为:c(M)=1molL﹣1 , c(N)=0.3molL﹣1;达到平衡后,M的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学﹣﹣选修5有机化学基础]I.已知有机物A仅含碳、氢、氧3种元素,质谱分析可知其相对分子质量为46,核磁共 振氢谱显示分子中有三种不同化学环境的氢原子,且有如下的转化关系:
(1)由A→B的反应类型是
(2)D的红外光谱表明分子内除C一H键、C一C键外还含有两个C一O单键,反应①中 D与HCl按物质的量之比1:1反应,则D的结构简式是II.化合物E和F是药品普鲁卡因合成的重要原料,普鲁卡因的合成路线如下:已知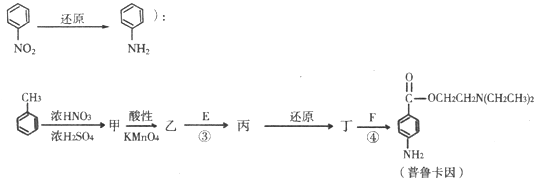
(3)丁的结构简式为
(4)反应③的化学方程式是
(5)普鲁卡因有两种水解产物戊和己,且戊与甲具有相同的分子式.符合下列条件的戊的同分异构体有种(包含戊);a.分子结构中含苯环,且每个苯环有2个侧链
b.分子结构中一定含官能团一NH2且一NH2直接与碳原子相连
(6)戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域.该聚合反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下操作不合理的是
A.用硫粉覆盖地下撒有的汞B.用二氧化碳扑灭金属钠引起的失火
C.用热碱溶液洗去试管内壁的硫D.用湿的红色石蕊试纸检验氨气是否集满
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com