
【题目】请根据所学知识回答下列问题:
(1)同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1____________ΔH2(填“>”“<”或“=”下同)。
(2)相同条件下,2 mol氢原子所具有的能量____________1 mol 氢分子所具有的能量。
(3)已知:常温下,0.01 mol·L-1 MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol可溶正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为_______________
(4)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:
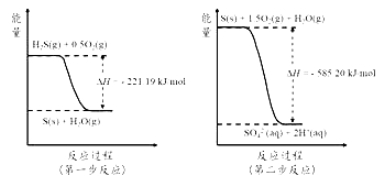
1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为______________________。
(5)一定条件,在水溶液中1 mol Cl-、ClO x-(x=1,2,3,4)的能量(KJ)相对大小如图所示。
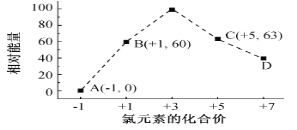
①D是______________________ (填离子符号)。
②B→A+C反应的热化学方程式为______________________ (用离子符号表示)。
【答案】
(1)=;(2)>;(3)ΔH=+45.2 kJmol-1;
(4)H2S(g)+2O2(g)=SO42-(aq)+H+(aq) ΔH=-806.39 kJmol-1
(5)①ClO4-;②3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol;
【解析】
试题分析:
(1)反应热与反应物的总能量和生成物的总能量,与反应条件无关,则光照和点燃条件的△H相同。
(2)氢气分子生成氢原子要破坏化学键,需要吸热,则2mol氢原子所具有的能量大于1mol氢分子所具有的能量。
(3)常温下,0.01molL-1 MOH溶液的pH为10,说明MOH是弱碱:MOH(aq)+H+(aq)═M+(aq)+H2O(l)△H1=-12.1 kJmol-1①,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3 kJmol-1②,根据盖斯定律,由①-②得:MOH(aq)M+(aq)+OH-(aq)△H=(-12.1+57.3)kJmol-1=+45.2 kJmol-1。
(4)由两步反应的能量变化示意可以看出,H2S先被氧化为S(s)释放能量,H2S(g)+0.5O2(g)===S(s)+H2O(g) ΔH =-221.19 kJ·mol-1,然后S再被进一步氧化为 SO42-(aq)释放能量:S(s)+1.5O2(g)+H2O(g)===SO42-(aq)+ 2H+(aq) ΔH =-585.20 kJ·mol-1,根据盖斯定律,将两个热方程式相加可得1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式,即:H2S(g)+2O2(g)=SO42-(aq)+H+(aq) ΔH=-806.39 kJmol-1
(5)①根据图象知,D中Cl元素化合价为+7价,所以ClOx-中x为4,则D为ClO4-;②B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol,所以该热化学反应方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某温度下,将2molA和3molB充入一密闭的容器中发生反应:aA(g)+B(g)![]() C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
A. a="3" B. a="2" C. B的转化率为40% D. B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关方程式书写正确的是
A.FeCl2溶液中加入氯水的离子方程式:Fe2++ Cl2=Fe3++2Cl-
B.食醋与NaOH反应的离子方程式:H++OH-=H2O
C.CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.Na2O2与水反应的离子方程式:2O22-+ 2H2O = 4OH-+ O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学,下列说法不正确的是
A. 明矾可作净水剂 B. 生石灰用于食品抗氧化剂
C. 用热碱水清除炊具上残留的油污 D. 用浸泡过高锰酸钾溶液的硅藻土保存水果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-) 根据图示判断,下列说法正确的是

A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C.欲使NaHA溶液呈中性,可以向其中加入酸或碱
D.向NaHA溶液加入水的过程中,pH可能增大也可能减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①NaHCO3 ②Na2CO3 ③Al2O3 ④Fe(OH)3 ⑤Al(OH)3 ⑥CO2 ⑦FeCl3 ⑧FeCl2 ⑨MgCl2 ⑩N2 Na2SO4·10 H2O
(1)其中既能跟稀H2SO4反应,又能跟NaOH溶液反应的是 (填序号),
(2)除去固体②中的固体①的方法是 ;
(3)在同温同压下,测得⑩与⑥混合气体对氢气的相对密度为18,⑩的⑥体积之比为 ;
(4)欲配制250 mL0. 1 mol/L的Na2SO4溶液需要称量的质量为 g ;
(5)在①④⑤⑧中可以通过化合反应得到的物质有 (填序号);
(6)要除去⑦溶液中的少量⑧,可行的办法是
A.滴入KSCN溶液 B.加入氯水 C.加入铜粉 D.加入铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用3mL稀硫酸溶液与足量Zn反应,当气泡稀少时加入5mL浓硫酸,又迅速产生较多气泡,由上述操作及现象得出结论:硫酸浓度增大,产生H2的反应速率加快
B.FeCl3+3KSCN![]() Fe(SCN)3(血红色) +3KCl,向溶液中加入KCl固体可快速看到血红色
Fe(SCN)3(血红色) +3KCl,向溶液中加入KCl固体可快速看到血红色
C.Ba(OH)2·8H2O与NH4Cl的反应是放热反应
D.化学反应中的能量变化,通常表现为热量的变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com