
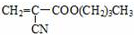 .其合成方法之一的路线如下:
.其合成方法之一的路线如下: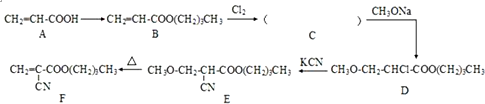
 .
. 分析 (1)根据A的结构简可知,A与钠发生置换反应生成氢气;
(2)B中含有碳碳双键和酯基,酯基能与氢氧化钠溶液反应,碳碳双键与溴化氢加成反应、被酸性高锰酸钾氧化;
(3)B与氯气加成得到C,C中端碳上的氯原子与CH3ONa发生取代反应生成D,C的结构简式为ClCH2CHClCOO(CH2)3CH3;
(4)从E、F两种物质结构,判断E中相邻碳原子失去甲氧基和氢原子生成碳碳双键,故反应为消去反应;
(5)该物质中含有碳碳双键,能发生加聚反应生成高聚物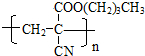 .
.
解答 解:(1)A与金属钠反应的化学方程式为2CH2=CHCOOH+2Na→CH2=2CHCOONa+H2↑,
故答案为:2CH2=CHCOOH+2Na→CH2=2CHCOONa+H2↑;
(2)B中含有碳碳双键和酯基,酯基能与氢氧化钠溶液反应,碳碳双键与溴化氢加成反应、被酸性高锰酸钾氧化,不能与钠反应,故选:bcd;
(3)B与氯气加成得到C,C中端碳上的氯原子与CH3ONa发生取代反应生成D,C的结构简式为ClCH2CHClCOO(CH2)3CH3,分子式为:C7H12O2Cl2,
故答案为:C7H12O2Cl2;
(4)从E、F两种物质结构,可知E中相邻碳原子失去甲氧基和氢原子,生成碳碳双键,故反应为消去反应,
故答案为:消去反应;
(5)该物质中含有碳碳双键,能发生加聚反应,反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,是对有机化学的综合考查,注意根据有机物的结构进行分析解答,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用青霉素时,有些人可以不进行皮肤敏感试验 | |
| B. | 长期大量使用阿司匹林可预防疾病,没有副作用 | |
| C. | 对于标记“OTC”的药物,必需在医生指导下使用 | |
| D. | “是药三分毒”,必须按医嘱或药物说明书使用药物,防范药物不良反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-、ClO-在酸性溶液中不能大量共存 | |
| B. | 在无色碱性溶液中:ClO、Cl-、Fe2+、Na+能大量共存 | |
| C. | 洁厕灵(主要成分是盐酸)和84消毒液(主要成分是次氯酸钠)混合使用效果更好 | |
| D. | 符合该离子方程式的化学方程式可以是:HClO+HCl=Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O作呼吸面具中的供氧剂 | B. | 小苏打做发酵粉 | ||
| C. | 镁合金用于制造汽车、飞机、火箭 | D. | 漂白粉做消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质硅可用于制造光纤制品 | B. | 碳酸氢钠常用于焙制糕点 | ||
| C. | 氧化铝可用于制造耐火坩埚 | D. | 氢氧化铝常用于治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳的燃烧热△H<-110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀硫酸与稀NaOH溶液反应的中和热△H=-2×57.3 kJ/mol | |
| D. | 稀醋酸和稀NaOH溶液反应生成1 mol H2O,放出57.3 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验数据或现象 | 结论 | |
| A | 用PH计分别测定SO2和CO2饱和溶液的PH | 前者PH小 | H2SO3酸性强于H2CO3 |
| B | 向Ag Cl悬浊液中加入NaI溶液 | 产生黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| C | 向滴用酚酞的氨水中加入少量CH3COONH4固体 | 溶液红色变浅 | 氨水中存在电离平衡 |
| D | 等体积、等PH的HA和HB两种酸溶液分别与足量的锌反应 | 相同时间内,HA酸产生的氢气多 | HA是强酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com