
下列叙述正确的是( )
A.高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强
B.陶瓷、玻璃、水泥容器都能贮存氢氟酸
C.石灰抹墙、水泥砌墙的硬化过程原理相同
D.玻璃熔炉中出来的气体的主要成分是二氧化碳
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有4个电子。
(1)D原子的电子排布式为 ,若A元素的原子最外层电子排布为1s1,
则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于 键。
(2)当n=2时,B的原子结构示意图为 ,B与C形成的晶体属于 晶体。
当n=3时,B与C形成的晶体属于 晶体。
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A
在周期表中的位置是 ,A、B、C、D四种元素的电负性由大到小的顺序
是 (用元素符号表示)。
(4)C和D的最简单氢化物相比较:稳定性: (填化学式,下同);沸点: 原是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验必须注意安全,下列说法不正确的是 ( )
A. 不慎将酸液溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
B. 不慎将碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
C. 洒在桌面上的酒精燃烧,立即用湿抹布盖灭
D. 配置硫酸溶液时,可先在量筒中加入一定体积的水,在慢慢倒入浓硫酸,并搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行反应:X2(g)+Y2(g)
 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A.Z为0.3 mol·L-1 B.Y2为0.4 mol·L-1
C.X2为0.2 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将2 mol A和1 mol B两种气体相混合于体积为2 L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g)
 xC(g)+2D(g)ΔH<0,2 min末反应达到平衡状态(温度不变),生成了1mol D,并测得C的浓度为0.5 mol·L-1,请填写下列空白:
xC(g)+2D(g)ΔH<0,2 min末反应达到平衡状态(温度不变),生成了1mol D,并测得C的浓度为0.5 mol·L-1,请填写下列空白:
(1)x的值等于________________。
(2)该反应的化学平衡常数K=________,升高温度时K值将________(选填“增大”、“减小”或“不变”)。
(3)A物质的转化率为__________________。
(4)若维持温度不变,在原平衡混合物的容器中再充入2mol C和2mol D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关玻璃的说法不正确的是( )
A.制普通玻璃的原料主要是纯碱、石灰石和石英
B.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅
C.玻璃在加热熔化时有固定的熔点
D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅反应生成硅酸钠而使瓶塞与瓶口粘在一起
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子组一定能大量共存的是( )
A.酚酞呈红色的溶液中:Al3+、Cl-、N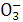 、Na+
、Na+
B.石蕊呈蓝色的溶液中:Na+、[Al(OH)4]-、N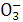 、HC
、HC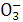
C.含大量Al3+的溶液中:K+、Na+、N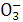 、ClO-
、ClO-
D.含大量OH-的溶液中:C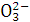 、Cl-、F-、K+
、Cl-、F-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积为2 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
| T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)Q____0(填 “>”、“<”),升高温度,化学平衡向________(填“正反应”或“逆反应”)方向移动。
(2)若某温度下,平衡浓度符合下列关系:c(CO2)·c(H2)=c(CO)·c(H2O),此时的温度为__________;在此温度下,若该容器中含有1mol CO2、3mol H2、2mol CO、2mol H2O,则此时反应所处的状态为____________(填“向正反应方向进行中”、“向逆反应方向进行中”或“平衡状态”),此温度平衡时CO2的浓度为___________ mol·L-1;在此温度下,若该容器中含有1.5mol CO2、3.5mol H2、1.5mol CO、1.5mol H2O达到平衡时CO2的浓度为___________ mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com