
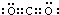 或
或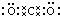 ,故答案为:
,故答案为: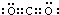 或
或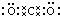 ;
;

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
①b+c![]() Y ②a+c
Y ②a+c![]() Z ③X+Y
Z ③X+Y![]() M ④X+Z
M ④X+Z![]() c+N ⑤Y+Z
c+N ⑤Y+Z![]() c+N
c+N
完成下列问题:
(1)上述反应中一定属于氧化还原反应的是____________________________(填序号),其理由是____________________________________________________________________。
(2)如果M是一种无色、黏稠的油状液体,则X、Y、Z分别为_______________、____________、____________,写出反应的化学方程式:
③______________________________________________,
④______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.B+C![]() Y; Ⅱ.A+C
Y; Ⅱ.A+C![]() Z; Ⅲ.X+Y
Z; Ⅲ.X+Y![]() M; Ⅳ.X+Z
M; Ⅳ.X+Z![]() C+N; Ⅴ.Y+Z
C+N; Ⅴ.Y+Z![]() C+N
C+N
(1)上述反应中,一定属于氧化还原反应的是______________。(填反应编号)
(2)如果化合物M是一种无色黏稠油状液体,则X、Y的化学式分别是______________、______________。
(3)Z的电子式为______________。
(4)写出反应Ⅲ的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
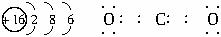
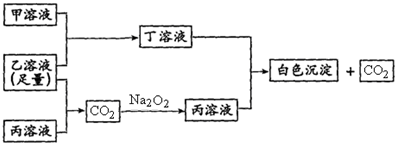
请回答:?
(1)写出C元素的原子结构示意图,写出丁和戊的电子式_________、________;丁在固态时属于___________晶体。
(2)用有关化学用语解释:
①乙溶液呈酸性的原因____________________;
②丙溶液呈碱性的原因____________________。
(3)写出有关反应的离子方程式:?
①乙溶液+丙溶液→丁__________________;?
②己溶液+丙溶液→丁__________________。?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com