
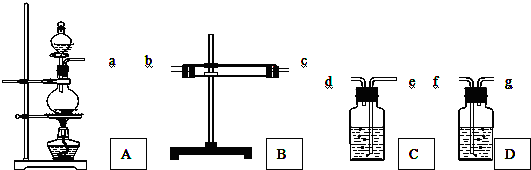
分析 浓硫酸和铜在加热条件下发生氧化还原反应生成硫酸铜、先在B中用无水硫酸铜检验水,在C中用品红溶液检验二氧化硫,D为二氧化硫的尾气吸收装置,防止污染空气,以此解答该题.
解答 解:(1)检验水用无水硫酸铜,检验SO2用品红溶液,因此先检测水,再检测SO2,氢氧化钠溶液用于吸收多余的SO2,C、D中均长进短出,顺序为a→b→c→e→d→f,
故答案为:b;c;e;d;f;
(2)B中白色的无水硫酸铜变为蓝色,说明产物有水,二氧化硫具有漂白性,可使品红溶液褪色,因此C中的品红溶液褪色证明产物中含有SO2,如果C装置放在B之前,则不能检验出反应是否有水生成,
故答案为:白色固体变为蓝色;品红褪色;如果C装置放在B之前,则不能检验出反应是否有水生成;
(3)氢氧化钠溶液用于吸收多余的二氧化硫气体,防止空气污染,
故答案为:吸收多余的SO2,防止污染大气;
(4)铜与浓硫酸在加热的条件下反应生成硫酸铜、SO2和H2O,化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
点评 本题考查了浓硫酸与铜反应产物的验证实验,为高考常见题型,侧重于学生的分析、实验能力的考查,题目难度中等,涉及仪器的选择和组装、物质的检验方法顺序的选择以及环境保护等问题,化学方程式的书写时要注明浓硫酸.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用铂丝蘸取少量某溶液进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色,该溶液一定是钾盐溶液 | |
| B. | 在0.1mol•L-1Na2CO3溶液中,加两滴酚酞显浅红色,微热后红色加深,说明盐类水解反应是吸热反应 | |
| C. | 向某FeCl2 溶液中加入KSCN溶液,观察到溶液呈血红色,说明该溶液中FeCl2已全部被氧化 | |
| D. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的分子大小不同 | B. | 气体的物质的量不同 | ||
| C. | 气体的性质不同 | D. | 气体的分子间距离不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消耗盐酸一样多 | B. | 放出CO2一样多 | ||
| C. | 消耗盐酸后者多 | D. | 后者放出CO2的量是前者的一半 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 起始浓度/mol•L-1 | 3 | 1 | 0 |
| 2s末浓度/mol•L-1 | 1.8 | 0.6 | 0.8 |
| A. | 0.4 mol•L-1•s-1 | B. | 0.2 mol•L-1•s-1 | C. | 0.8 mol•L-1•s-1 | D. | 0.6 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常用明矾或硫酸铝做净水剂 | |
| B. | 实验室将氯化铁晶体溶于浓盐酸来配制饱和氯化铁溶液 | |
| C. | 用热的纯碱液清洗餐具表面的油污比用冷的溶液效果好 | |
| D. | 泡沫灭火器中用NaHCO3溶液和Al2(SO4)3溶液发生反应产生CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.3 | B. | 8.7 | C. | 9.3 | D. | 9.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com