
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
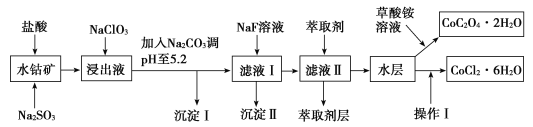
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀Ⅰ中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3目的是___。
(2)NaClO3在浸出液中发生反应的离子方程式为___。
(3)加入Na2CO3调pH至5.2,目的是___;萃取剂层含锰元素,则沉淀Ⅱ的主要成分为__。
(4)操作Ⅰ包括:将水层加入浓盐酸调整pH为2~3,___、__、过滤、洗涤、减压烘干等过程。
(5)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中CoCl2·6H2O质量分数大于100%,其原因可能是___(回答一条原因即可)。
(6)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为____。[已知:CoC2O4·2H2O的摩尔质量为183g·mol1]
【答案】将Fe3+、Co3+还原 ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O 使Fe3+和Al3+沉淀完全 CaF2和MgF2 蒸发浓缩 冷却结晶 粗产品中结晶水含量低(或粗产品中混有氯化钠杂质) Co3O4(或CoO·Co2O3)
【解析】
(1)、浸出过程中,Co2O3、Fe2O3与盐酸、Na2SO3发生反应,Co2O3转化为Co2+,Fe2O3转化为Fe2+,Co、Fe元素化合价降低,则S元素化合价升高,SO32-转化为SO42-,故答案为:将Fe3+、Co3+还原;
(2)、NaClO3加入浸出液中,将Fe2+氧化为Fe3+,ClO-被还原为Cl-,反应的离子方程式为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O-;
(3)根据工艺流程图结合表格中提供的数据可知,加Na2CO3调pH至5.2,目的是使Fe3+和Al3+沉淀完全。滤液l中含有的金属阳离子为Co2+、Mn2+、Mg2+、Ca2+等,萃取剂层含锰元素,结合流程图中向滤液1中加入了NaF溶液,知沉淀Ⅱ为MgF2、CaF2;
(4)、经过操作I由溶液得到结晶水合物,故除题中已知过程外,操作I还包括蒸发浓缩、冷却结晶;
(5)、根据CoCl2·6H2O的组成及测定过程分析,造成粗产品中CoCl2·6H2O的质量分数大于100%的原因可能是:含有氯化钠杂质,使氯离子含量增大或结晶水合物失去部分结晶水,导致相同质量的固体中氯离子含量变大;
(6)、整个受热过程中只产生水蒸气和CO2气体,5.49 g CoC2O4·2H2O为0.03mol,固体质量变为4.41 g时,质量减少1.08g,恰好为0.06 mol H2O的质量,因此4.41 g固体为0.03 mol CoC2O4。依据元素守恒知,生成n(CO2)=0.06 mol,m(CO2)=0.06mol×44 g/mol=2.64 g。而固体质量由4.41 g变为2.41 g时,质量减少2 g,说明290~320℃内发生的不是分解反应,参加反应的物质还有氧气。则参加反应的m(O2)=2.64 g-2 g=0.64 g,n(O2)=0.02mol,n(CoC2O4) : n(O2) : n(CO2)=0.03 : 0.02 : 0.06=3 : 2 : 6,依据原子守恒,配平化学方程式![]() ,故290~320℃温度范围,剩余固体物质的化学式为Co3O4或CoO·Co2O3。
,故290~320℃温度范围,剩余固体物质的化学式为Co3O4或CoO·Co2O3。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
【题目】已知:① CH3CH=CHCH2CH3![]() CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
② R-CH=CH2![]() R-CH2-CH2-Br
R-CH2-CH2-Br
香豆素的核心结构是芳香内酯A,A经下列步骤转变为水杨酸。
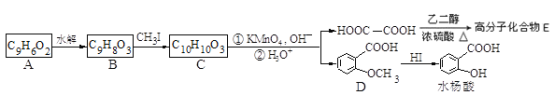
请回答下列问题:
(1)下列有关A、B、C的叙述中不正确的是___________
a. C中核磁共振氢谱共有8种峰
b. A、B、C均可发生加聚反应
c. 1mol A最多能和5mol氢气发生加成反应
d. B能与浓溴水发生取代反应
(2)B分子中有2个含氧官能团,分别为______和______(填官能团名称),B→C的反应类型为_____________。
(3)在上述转化过程中,反应步骤B→C的目的是_________________________。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的对二取代物,且水解后生成的产物之一能发生银镜反应。请写出其中一种的结构简式:_____________。
(5)写出合成高分子化合物E的化学反应方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间有如下转化关系: 下列有关物质的推断不正确的是 ( )
下列有关物质的推断不正确的是 ( )
A. 若甲为AlC13溶液,则丁可能是NaOH溶液 B. 若甲为N2,则丁可能是O2
C. 若甲为Fe,则丁可能是稀硝酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。用0.1 mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法正确的是( )
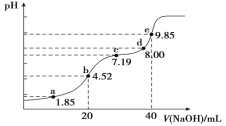
A.a点所得溶液中:2c(HSO3-)+c(SO32-)=0.1 mol/L
B.b点所得溶液中:c(H+)+c(SO32-)=c(OH-)+c(H2SO3)
C.c点所得溶液中:c(Na+)>3c(HSO3-)
D.d点所得溶液中:c(Na+)>c(OH-) >c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是周期表的一部分,根据元素在周期表中位置回答下列问题:
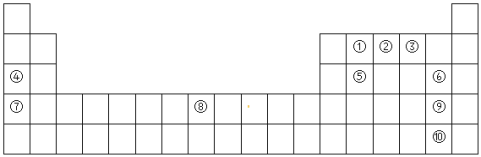
(1)元素⑤在周期表中的位置描述为_____________________,元素⑧的元素符号______。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是_____________(填化学式)。
(3)元素②的单质的电子式___________,元素②的简单氢化物与其最高价氧化物的水化物反应的生成物中含有的化学键______________________,元素①、②、③的简单氢化物的沸点由高到低的顺序是__________________________(用化学式表示)。
(4)非金属性比较:
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为______________
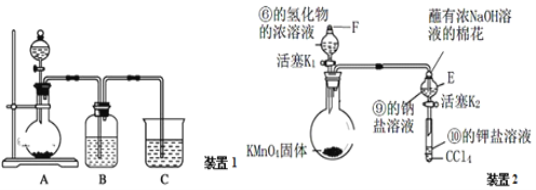
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验______(填“能”或“不能”)证明非金属性⑥>⑨>⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的乙醇电池,它用磺酸类质子溶剂。电池总反应为:C2H5OH +3O2→ 2CO2+3H2O,电池示意如图,下列说法正确的是

A. a极为电池的正极
B. 电池工作时电流由a极沿导线经灯泡再到b极
C. 电池负极的电极反应为:4H++ O2+ 4e-= 2H2O
D. 电池工作时,1mol乙醇被氧化时就有12mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里迅速制备少量氯气可利用以下反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)用双线桥法表示出电子转移的方向和数目__________。2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(2)该反应中,氧化剂是__________,还原剂是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 相同温度下,同时向 ①4 mL 0.1 molL-1 KMnO4酸性溶液和②4 mL 0.2 molL-1 KMnO4酸性溶液中,分别加入4 mL 1 molL-1 H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
B | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
C | 加热2NO2(g) | 颜色加深 | 证明正反应是放热反应 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.NaHS在水中的电离方程式为NaHS=Na++HS﹣,HS﹣![]() H++S2﹣
H++S2﹣
B.氧化还原反应中,一种元素被氧化的同时必有另一种元素被还原
C.1mol配合物Fe(CO)5(羰基铁)中含有5mol配位键
D.氢氧化铁胶体带有正电荷,通电时向电源负极一端移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com