
【题目】痛灭定钠是一种吡咯乙酸类的非甾体抗炎药,其合成路线如图:
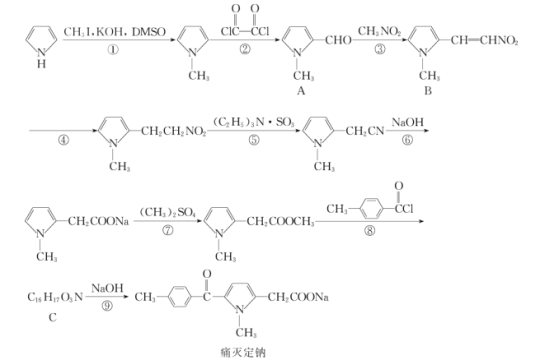
回答下列问题:
(1)化合物B中含有官能团的名称是__。
(2)化学反应①和④的反应类型分别为__和__。
(3)化合物C的结构简式为__。
(4)下列关于痛灭定钠的说法错误的是__。
a.与溴充分加成后官能团种类数不变
b.能够发生水解反应
c.核磁共振氢谱分析能够显示6个峰
d.可使溴的四氯化碳溶液褪色
e.1mol痛灭定钠与氢气加成最多消耗3molH2
(5)反应⑦的化学方程式为__。
(6)芳香族化合物X的相对分子质量比A大14,写出遇FeCl3溶液显紫色且取代基仅位于苯环对位上化合物X的结构简式:__(不考虑立体异构)。
(7)根据该试题提供的相关信息,写出由化合物![]() 及必要的试剂制备有机化合物
及必要的试剂制备有机化合物![]() 的合成路线图。__。
的合成路线图。__。
【答案】碳碳双键、硝基 取代反应 加成反应 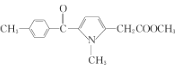 ce 2
ce 2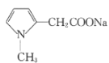 +(CH3)2SO4→2
+(CH3)2SO4→2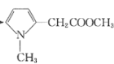 +Na2SO4
+Na2SO4 ![]() 、
、![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】
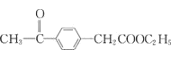
根据合成路线分析:![]() 与CH3I发生取代反应①转变为
与CH3I发生取代反应①转变为![]() ,
,![]() 发生反应②,在邻位引入醛基转变为:
发生反应②,在邻位引入醛基转变为: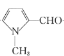 ,
,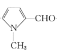 与CH3NO2发生反应生成
与CH3NO2发生反应生成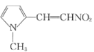 ,
,![]() 与氢气发生加成反应生成
与氢气发生加成反应生成![]() ,
,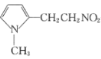 发生反应⑤将CH2NO2脱去氢氧原子转变为CN,生成
发生反应⑤将CH2NO2脱去氢氧原子转变为CN,生成 ,反应⑥中CN碱性水解转变成COONa,得到
,反应⑥中CN碱性水解转变成COONa,得到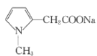 ,
,![]() 反应生成
反应生成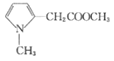 ,
,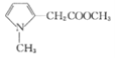 与
与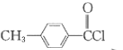 发生取代反应生成
发生取代反应生成 ,
,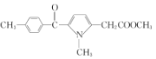 在碱性条件下水解得到
在碱性条件下水解得到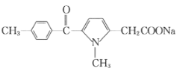 ,据此作答。
,据此作答。
(1)由B的结构简式可知其中含有的官能团为:碳碳双键和硝基;
答案为:碳碳双键、硝基;
(2)由上述分析可知反应①为取代反应,④为加成反应;
答案为:取代反应;加成反应;
(3)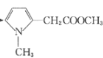 与
与 发生取代反应生成C为
发生取代反应生成C为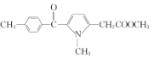 ,答案为:
,答案为: ;
;
(4)a.与溴充分加成后碳碳双键消失,引入了溴原子,故官能团种类数不变,a正确;
b.结构中存在COONa,属于弱酸盐结构,能够发生盐类的水解反应,b正确;
c.该结构中有7种氢,故核磁共振氢谱分析能够显示7个峰,c错误;
d.该结构中含碳碳双键能与溴单质发生加成反应,使溴的四氯化碳溶液褪色,d正确;
e.苯环、碳碳双键和羰基都可以与氢气加成,因此1mol痛灭定钠与氢气加成最多消耗6molH2,e错误;
答案为:ce;
(5)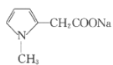 反应生成
反应生成 ,反应方程式为:2
,反应方程式为:2 +(CH3)2SO4→2
+(CH3)2SO4→2 +Na2SO4;
+Na2SO4;
故答案为:2 +(CH3)2SO4→2
+(CH3)2SO4→2 +Na2SO4;
+Na2SO4;
(6)芳香族化合物说明X中有苯环,相对分子质量比A大14,说明比A多一个CH2,且与A的不饱和度相同;遇FeCl3溶液显紫色说明含有酚羟基;取代基仅位于苯环对位上说明有两个取代基且为对位关系,满足条件的结构简式有:![]() 、
、![]() ,
,
故答案为:![]() 、
、![]() ;
;
(7)完全仿照题干中框图中反应⑥⑦⑧,选择合适试剂即可完成,![]() 与氢氧化钠水解得到苯乙酸钠,苯乙酸钠与(CH3CH2)2SO4反应得到
与氢氧化钠水解得到苯乙酸钠,苯乙酸钠与(CH3CH2)2SO4反应得到![]() ,
,![]() 再与乙酰氯反应生成
再与乙酰氯反应生成 ,合成路线为:
,合成路线为:![]()
![]()
![]()
![]()
![]()
![]()
 ;
;
故答案为:![]()
![]()
![]()
![]()
![]()
![]()
 。
。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如图:
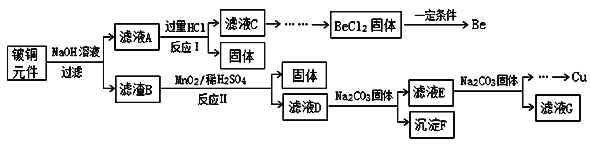
已知:I、铍、铝元素化学性质相似;
Ⅱ、常温下部分难溶物的溶度积常数如表:
难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)滤液A的主要成分除NaOH、Na2BeO2外,还有___________(填化学式),写出反应I中Na2BeO2与过量盐酸反应的离子方程式:________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,最合理的实验步骤顺序为_______(填字母)
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH d.加入适量的HCl e.洗涤 f.过滤
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:___________。若用浓HNO3溶解金属硫化物,缺点是_______(任写一条)。
(4)滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=8.0×10-3mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入Na2CO3溶液调节pH可将其转变成氢氧化物依次分离,首先沉淀的是_______(填离子符号);为使铜离子开始沉淀,常温下应调节溶液的pH大于______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表:下列说法错误的是:( )
物质 | X | Y | Z |
初始浓度/ | 0.1 | 0.2 | 0 |
平衡浓度/ | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.改变温度可以改变此反应的平衡常数
D.增压使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列装置模拟“侯氏制碱法”,通过制备的NH3和CO2,与饱和食盐水反应先制备NaHCO3。下列说法正确的是( )
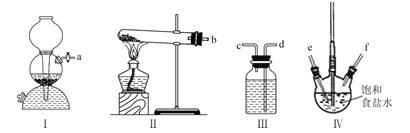
A.实验时装置I产生的气体应先通人到装置IV中
B.装置II中的试剂为浓硫酸
C.导管口的连接顺序为a-e-f-d-c-b
D.实验过程中,装置IV内会出现浑浊现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荣获2019年诺贝尔化学奖的吉野彰是最早开发具有商业价值的锂离子电池的日本科学家,他设计的可充电电池的工作原理示意图如图所示。该可充电电池的放电反应为LixCn+Li(1-x)CoO2=LiCoO2+nC。NA表示阿伏伽德罗常数的值。下列说法错误的是( )
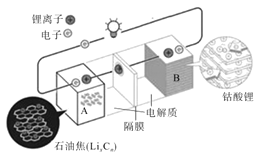
A.该电池用于电动汽车可有效减少光化学烟雾污染
B.充电时,正极反应为LiCoO2-xe-=Li(1-x)CoO2+xLi+
C.放电时,Li+由A极移向B极
D.若初始两电极质量相等,当转移2NA个电子时,两电极质量差为14g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、理象和结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向某溶液中加入NaOH 溶液,并用湿润的红色石蕊试纸检验 | 试纸没有变蓝 | 原溶液中没有有NH4+ |
B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
C | 向某溶液中滴加氯水后,再加KSCN溶液 | 溶液变红 | 原溶液中一定有Fe2+ |
D | 向某无色溶液中滴加BaCl2溶液 | 产生白色沉淀 | 该无色溶液中一定含有SO42- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,总反应为2Na+xS![]() Na2Sx,其反应原理如图所示。下列叙述正确的是( )
Na2Sx,其反应原理如图所示。下列叙述正确的是( )
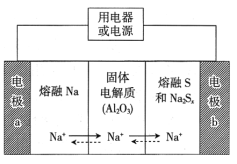
A.放电时,电极a为正极
B.放电时,内电路中Na+的移动方向为从b到a
C.充电时,电极b的反应式为Sx2--2e-=xS
D.充电时,Na+在电极b上获得电子,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数约为6.02×![]()
![]() ,下列叙述不正确的是( )
,下列叙述不正确的是( )
A.将1 mol ![]() 转化为
转化为![]() 胶体,
胶体,![]() 胶粒数小于6.02×
胶粒数小于6.02×![]()
B.标准状况下,22.4 L![]() 中含有溴原子数约为2×6.02×
中含有溴原子数约为2×6.02×![]()
C.常温下,9.2 g ![]() 含有的分子数小于0.2×6.02×
含有的分子数小于0.2×6.02×![]()
D.25℃时,pH=12的![]() 溶液1 L所含
溶液1 L所含![]() 数约为6.02×
数约为6.02×![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com