
 氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:
氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:| A. | 反应开始时速率增大可能是c(H+)所致 | |
| B. | 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合 | |
| C. | 纵坐标为v(H+)的v-t曲线与图中曲线完全重合 | |
| D. | 后期反应速率下降的主要原因是反应物浓度减小 |
分析 由题目信息可知反应的速率随c(H+)的增大而加快;根据电子得失守恒和原子守恒配平方程式,然后根据速率之比等于化学计量数之比可判断v-t曲线与图中曲线是否重合,随着反应的进行,浓度减小,则反应速率减小,以此解答该题.
解答 解:A.由方程式:ClO3-+HSO3--SO42-+Cl-+H+可知:反应开始时随着反应的进行,c(H+)不断增大,反应的速率加快由题目信息可知反应的速率随c(H+)的增大而加快,故A正确;
B.在反应中ClO3-+HSO3--SO42-+Cl-+H+,1molClO3-参加氧化还原反应得到6mol电子,1mol亚硫酸氢根离子参加氧化还原反应失去2mol电子,所以得失电子的最小公倍数是6,则ClO3-的计量数是1,亚硫酸氢根离子的计量数是3,其它原子根据原子守恒来配平,所以该方程式为:ClO3-+3HSO3-=3SO42-+Cl-+3H+,v(ClO3-):v(Cl-)=1:1,纵坐标为v(Cl-)的v-t曲线与图中曲线重合,故B正确;
C.该方程式为:ClO3-+3HSO3-=3SO42-+Cl-+3H+,v(ClO3-):v(H+)=1:3,纵坐标为v(H+)的v-t曲线与图中曲线不重合,故C错误;
D.随着反应的进行,反应物的浓度减少,反应速率减小,所以后期反应速率下降的主要原因是反应物浓度减小,故D正确.
故选C.
点评 本题主要考查了外界条件对化学反应速率的有关知识,为高频考点,侧重于学生的分析、计算能力的考查,难度不大,需要注意的是要抓住题目的信息是解答A选项的关键.


科目:高中化学 来源: 题型:选择题
| A. | Cl2+2NaOH═NaCl+NaClO+H2O | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | CO2+NH3+H2O═NH4HCO3 | D. | 2Na2O2+2CO2═2Na2CO3+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①②⑤ | C. | ②⑤③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第二周期第IA族 | B. | 第三周期第IVA族 | C. | 第二周期第VA族 | D. | 第三周期第VA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cn是第六周期元素 | B. | Cn是过渡元素 | ||
| C. | Cn是非金属元素 | D. | Cn的一种核素可表示为165Cn |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤干馏得到的煤焦油,其主要用途就是再经蒸馏得到高品质燃油,这一做法可以体现“低碳生活”的理念 | |
| B. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| C. | 刚玉、红宝石、蓝宝石的主要成分是氧化铝,而青花瓷、石英玻璃、分子筛的主要成分是硅酸盐 | |
| D. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铊是两性氢氧化物 | B. | 铊能置换出盐酸中的氢 | ||
| C. | 铊是质软的银白色的金属 | D. | 铊能生成+3价的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
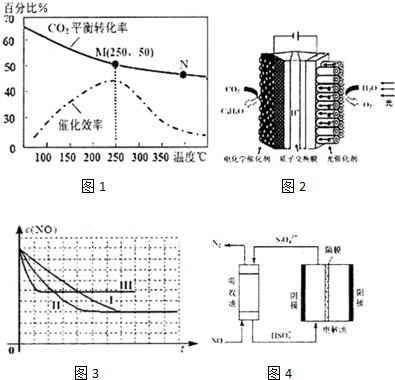
| 编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | a | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com