
| A、当调节溶液的pH至3.7时,Fe3+才能完全沉淀 |
| B、当c(OH-)达到10-9时,Cu2+开始沉淀,此时Fe3+尚未沉淀完全 |
| C、原溶液中,c(SO42-):[c(Cu2+)+c(Fe3+)]=4:3 |
| D、若要除去上述混合溶液中的Fe3+,加入NaOH固体比加入Cu(OH)2效果好 |


科目:高中化学 来源: 题型:
 (每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A、2molBr2 2molNaOH |
| B、2molBr2 3molNaOH |
| C、3molBr2 4molNaOH |
| D、4molBr2 4molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:


 也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式
也能发生类似V→Ⅵ的反应,请写出所生成醇的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用丁达尔现象区分淀粉溶胶和豆浆 |
| B、钠和水反应实验时,余下的金属钠放回原瓶 |
| C、浓硫酸与浓硝酸混合时,将浓硝酸加入浓硫酸中 |
| D、蒸发结晶时,把液体蒸干再停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
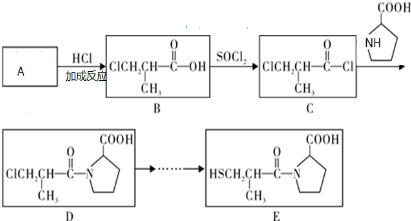
| NaOH |
| △ |
| H+ |
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷的燃烧热△H=-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 |
| B、一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-38.6kJ?mol-1 |
| C、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6kJ?mol-1 |
| D、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ca(OH2)反应的中和热△H=2×(-57.3)kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com