
| ��c |
| ��t |
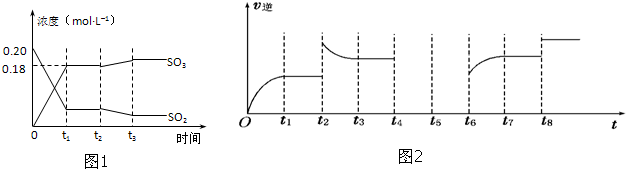
| c2(SO3) |
| c2(SO2)c(O2) |
| 0.09mol/L |
| 2min |
| c2(SO3) |
| c2(SO2)c(O2) |
| (0.18mol/L)2 |
| (0.02mol/L)2��0.01mol/L |
| 0.09mol/L |
| 0.1mol/L |
| (0.2x)2 |
| (0.2-0.2x)2��(0.1-0.1x) |
| (0.2x)2 |
| (0.2-0.2x)2��(0.1-0.1x) |
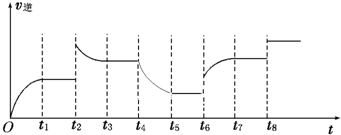
 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ˮ�м������NaOH��c��Na+��=c��Cl-��+c��ClO-��+c��OH-�� |
| B��pH=8.3��NaHCO3��Һ��c��Na+����c��H CO3 -����c��CO3 2-����c��H2CO3�� |
| C��pH=11�İ�ˮ��pH=3������������ϣ�c��Cl-��=c��NH4+����c��OH-��=c��H+�� |
| D��0.2 mol?L-1 CH3COOH��Һ��0.1 mol?L-1 NaOH��Һ�������ϣ�2c��H+��-2c��OH-��=c��CH3COO-��-c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 | B��4 | C��6 | D��8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B��������� |
| C��������� | D���˴Ź����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����롢�ᴿ----ȷ������ʽ-----ȷ��ʵ��ʽ----ȷ���ṹʽ |
| B�����롢�ᴿ----ȷ��ʵ��ʽ-----ȷ������ʽ-----ȷ���ṹʽ |
| C�����롢�ᴿ----ȷ���ṹʽ-----ȷ��ʵ��ʽ-----ȷ������ʽ |
| D��ȷ������ʽ-----ȷ��ʵ��ʽ----ȷ���ṹʽ-----���롢�ᴿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ɫ��ĩ�ijɷ� | �γɵ�ԭ�� |
| ������CaCO3�� | |
| ������ | ������½ϸߣ����ʵ��ܽ�Ƚ��ͻ��ܼ�������ʯ��ˮ�е����ʽᾧ������ |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | | �� | �� | �� |
| ʵ �� �� �� | ���ܹ۲쵽������ | �� �� |
| ȡ�����Թ��е��ϲ���Һ���μ�1��2��̪��Һ�� | ||
| �������Թ��в����Ĺ����м���ϡ���ᣮ | ��ɫ��ĩ�� ��ѡ��С����ޡ���CaCO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��2��7 |
| B��5��2��15 |
| C��1��6��13 |
| D��3��4��13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
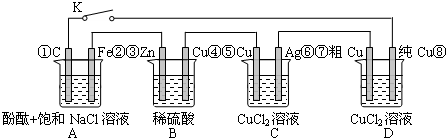
| A����K�պ�ʱ��Aװ�÷���������ʴ���ڵ�·������Դ |
| B����K�Ͽ�ʱ��Bװ��пƬ�ܽ⣬���������� |
| C����K�պϺ�������·�е��ӵ���������Ϊ�١��ࣻ�ߡ��ޣ��ݡ��ܣ��ۡ��� |
| D����K�պϺ�A��B��C��Dװ����pH����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com