
(10分)常温下,有下列7种溶液:A.Na2CO3 B.CH3COONa C.AlCl3
D.CH3COOH E.NaHCO3 F.NaOH G.HCl。
请回答有关问题:
(1)A溶液显碱性的离子方程式是: ;
(2)将C溶液蒸干灼烧后得到的固体是(写化学式): ;C与E是“泡沫灭火器”的药品,写出两溶液混合反应的离子方程式: ;
(3)若A、E两种溶液的pH相同,物质的量浓度大小关系是 。
(4)A、B、F溶液各25mL、物质的量浓度均为0.1mol/L,若分别加入25mL 0.1mol/L 的G溶液后,pH最大的是: 。(填“A、B或F”)
(1)CO32-+H2O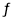 HCO3-+OH- (2)Al2O3 ; Al3++ 3HCO3- = Al(OH)3↓+3CO2↑
HCO3-+OH- (2)Al2O3 ; Al3++ 3HCO3- = Al(OH)3↓+3CO2↑
(3)E>A (4) A
【解析】
试题分析:(1)碳酸钠溶液是强碱弱酸盐,显碱性,水解的离子方程式是:CO32-+H2O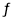 HCO3-+OH-;
HCO3-+OH-;
(2)AlCl3 溶液中存在AlCl3 +3H2O Al(OH)3 + 3HCl,盐酸易挥发,蒸干过程中盐酸挥发,导致平衡右移,生成氢氧化铝,灼烧后得到的固体是氧化铝;AlCl3 与NaHCO3 水解相互促进,生成气体和沉淀,能够作泡沫灭火器的药品,两溶液混合反应的离子方程式:Al3++ 3HCO3- = Al(OH)3↓+3CO2↑;
Al(OH)3 + 3HCl,盐酸易挥发,蒸干过程中盐酸挥发,导致平衡右移,生成氢氧化铝,灼烧后得到的固体是氧化铝;AlCl3 与NaHCO3 水解相互促进,生成气体和沉淀,能够作泡沫灭火器的药品,两溶液混合反应的离子方程式:Al3++ 3HCO3- = Al(OH)3↓+3CO2↑;
(3)根据越弱越水解,Na2CO3 与NaHCO3 ,碳酸钠的水解能力大于碳酸氢钠的水解能力,两种溶液的pH相同时,物质的量浓度大小关系是E>A 。
(4)Na2CO3、CH3COONa、NaOH溶液各25mL、物质的量浓度均为0.1mol/L,若分别加入25mL 0.1mol/L 的HCl溶液后,发生反应Na2CO3 +HCl=NaHCO3 +NaCl,碳酸氢钠溶液显碱性,CH3COONa+HCl=CH3COOH+NaCl,该混合溶液显酸性,NaOH+HCl=NaCl+H2O,溶液的显中性,pH最大的是A。
考点:考查盐类水解原理及应用,PH计算与大小比较等知识。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源:2014-2015山东省高二1月月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子一定能大量共存的是
A.滴加石蕊显红色的溶液中:Na+、Fe2+、Cl-、NO3-
B.[H+]=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
C.[OH-]/ [H+]=1012的溶液中:NH4+、Al3+、NO3-、CO32-
D.由水电离的[H+]=1.0×10-13 mol·L-1的溶液中:K+、NH4+、AlO2-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学文科试卷(解析版) 题型:填空题
(6分)化学无处不在,了解一些与食品相关的化学知识很有意义。
(1)薯片等容易挤碎的食品,宜选用充气袋装。袋装食品可充入的气体是________。
A.氮气 B.二氧化碳 C.氧气
(2)为使面包松软可口,通常用碳酸氢钠作发泡剂。因为它________。
①提供钠离子 ②增加甜味 ③与酸产生二氧化碳
A.②③ B.①③ C.①②
(3)苯甲酸钠(C6H5COONa)是常用的食品防腐剂。下列描述错误的是________。
A.苯甲酸钠属于盐类
B.苯甲酸钠能溶于水
C.苯甲酸钠属于烃类
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学文科试卷(解析版) 题型:选择题
下列常见材料中,属于有机高分子材料的是
A.橡胶 B.陶瓷 C.玻璃 D.水泥
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学理科试卷(解析版) 题型:填空题
(10分)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液c;M、N是两块电极板,通过导线与直流电源相连。

请回答以下问题:
(1)若M、N都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则: 极(填“M”或“N”)附近先呈红色;电解饱和NaCl溶液的总反应方程式: 。
(2)若要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
①N电极反应式是 。(说明:杂质发生的电极反应不必写出)
②下列说法正确的是________。
A.电能全部转化为化学能
B.在电解精炼中,电解液中有Al3+、Zn2+产生
C.溶液中Cu2+向阳极移动
D.阳极泥中可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为16g,则阳极上产生的气体在标准状况下的体积为 L 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学理科试卷(解析版) 题型:选择题
常温下,AgCl、AgBr、AgI的溶度积常数(Ksp)依次为1.8×10-10、5.4×10-13、8.5×10-17,下列说法错误的是
A.常温下在水中的溶解能力AgCl>AgBr>AgI
B.在AgCl饱和溶液中加入饱和NaBr溶液有AgBr沉淀生成
C.在AgI饱和溶液中加入饱和NaCl溶液有AgCl沉淀生成
D.将AgCl、AgBr和AgI的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,生成的AgI沉淀最多
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高二上学期期末化学理科试卷(解析版) 题型:选择题
相同条件下,等体积、等pH的醋酸溶液和盐酸分别加水稀释后,溶液的pH仍相同,则所得溶液的体积
A.仍相同 B.醋酸溶液的大 C.盐酸的大 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省师大一附高一上学期期中化学试卷(解析版) 题型:填空题
(4分)某氯化钾样品中含杂质硫酸钾,为了除去硫酸钾,要做以下6步实验:
A向滤液中滴加稀盐酸,边滴边振荡至不再产生气体
B将氯化钾样品溶于适量蒸馏水,配成溶液
C过滤,将白色沉淀滤出
D向溶液中滴加碳酸钾溶液边滴,边振荡至不再产生白色沉淀
E向溶液中滴加氯化钡溶液,边振荡至不再产生沉淀
F将滤液蒸干,得到晶体
(1)正确的实验操作程序为(填写序号)____________________
(2)进行F操作时用到的仪器主要有____________
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省唐山市高一上学期期中化学试卷(解析版) 题型:选择题
下列关于物质的量浓度表述正确的是
A.0.3 mol?L﹣1的Na2SO4溶液中含有Na+和SO42﹣的总物质的量为0.9 mol?L﹣1
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol?L﹣1,只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol?L﹣1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42﹣的物质的量相等,则K+和Cl﹣的物质的量浓度一定相同
D.10℃时,100 mL 0.35 mol?L﹣1的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol?L﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com