
| ||
| ||
| 8.7g |
| 87g/mol |
| n |
| V |
| ||
| 8.7g |
| 87g/mol |
| ||
| ||
| n |
| V |


科目:高中化学 来源: 题型:
| A、c(S2-)>c(HS-)>c(OH-)>c(H+) |
| B、c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| C、c(Na+)+c(H+)>c(HS-)+c(S2-)+c(OH-) |
| D、3c(S2-)+3c(HS-)+3c(H2S)=2c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
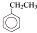
| CO4AlCl3.HCl |
| △ |
| M |
| OH- |
| -H2O |
| △ |
| C |
| (C11H12O) |
| ①Cu(OH)2 |
| ①酸化 |
| CH3OH |
| 浓H2SO4/△ |
| 催化剂 |
| F |
| (高聚物) |
 +CO
+CO| Al3.HCl |
| △ |
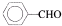
| OH- |
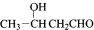
| -H2O |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙炔分子中有6个σ键,2个π键 |
| B、丙炔分子中3个碳原子都是sp杂化 |
| C、丙炔分子中只存在极性键 |
| D、丙炔分子中的π键比σ键稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
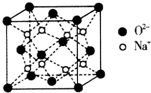 H、C、N、O、Na、Fe、Cu是常见的七种元素.
H、C、N、O、Na、Fe、Cu是常见的七种元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:Ca2+>Cl->S2- |
| B、非金属性:Si>C>N |
| C、电负性:F>S>Mg |
| D、热稳定性:CH4>H2S>NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
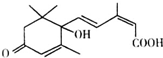 国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图.下列关于该物质的说法正确的是( )
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图.下列关于该物质的说法正确的是( )| A、该有机物的分子式为C15H21O4 |
| B、该有机物能发生取代、加成和水解反应 |
| C、1 mol该有机物与足量溴反应最多消耗4 mol Br2 |
| D、1 mol该有机物与足量Na反应生成1 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com