
| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL�� | 50 | 120 | 232 | 290 | 310 |
| 0.112L |
| 22.4L/mol |
| ||
| 1min |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ������I-Ũ���й� |
| B��IO-�Ǹ÷�Ӧ�Ĵ��� |
| C������Ӧ�ų�98 kJ������ʱ������1 mol O2 |
| D��v��H2O2��=v��H2O��=v��O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
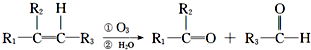
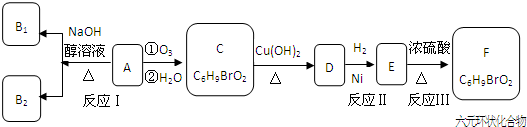
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ʵ������NaCl��������0.40mol/L��NaCl��Һ250mL��
ʵ������NaCl��������0.40mol/L��NaCl��Һ250mL���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
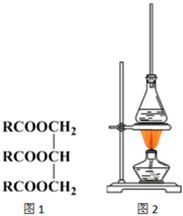 ��֬�Ǹ�֬����ĸ���������ṹ���Ա�ʾΪͼ1��RΪ��ͬ���ţ���������֬��������Ӧ�͵ζ������Բⶨ��֬��ƽ�����������ش��������⣺
��֬�Ǹ�֬����ĸ���������ṹ���Ա�ʾΪͼ1��RΪ��ͬ���ţ���������֬��������Ӧ�͵ζ������Բⶨ��֬��ƽ�����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������ | K+ Na+ Cu2+ Al3+ |
| ������ | SO42- HCO3-OH- Cl- |
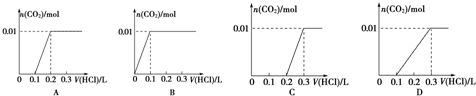
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��A��ƽ����Ӧ����Ϊ0.15mol/��L?min�� |
| B�����´ﵽƽ��ʱ������ѹǿΪ��ʼʱ��85% |
| C��B��ת����Ϊ10% |
| D��ƽ��ʱA��Ũ��Ϊ0.8mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������Һ�еμ������BaCl2��Һ��������ɫ��������˵�������к���SO42- |
| B��������Һ�еμ������BaCl2��Һ��������������˵�������в���SO42- |
| C��������ˮ�еμ�ϡHNO3��AgNO3��Һ��������ɫ��������˵������ˮ�к���Cl- |
| D��������ˮ�еμ�ϡHNO3��AgNO3��Һ��������ɫ��������˵������ˮ�к���Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com