
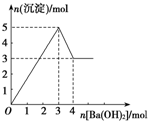
 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO4 | B. | KAl(SO4)2 | C. | Al2(SO4)3 | D. | Na AlO2 |
分析 A、氢氧化镁不溶于氢氧化钡溶液;
B、由图可知溶解氢氧化铝需要1mol氢氧化钡,由Al(OH)3+OH-=AlO2-+2H2O可知沉淀中Al(OH)3为2mol,加入3mol氢氧化钡沉淀最大,再加入氢氧化钡,又生成硫酸钡,且氢氧化铝会逐渐溶解,最终沉淀为4mol;
C、先发生反应Ba2++SO42-=BaSO4↓、Al3++3OH-═Al(OH)3↓,然后发生Al(OH)3+NaOH═NaAlO2+2H2O,由图可知溶解氢氧化铝需要1mol氢氧化钡,由Al(OH)3+OH-=AlO2-+2H2O可知沉淀中Al(OH)3为2mol,结合加入3mol氢氧化钡沉淀最大判断;
D、偏铝酸钠与氢氧化钡不反应.
解答 解:A、氢氧化镁不溶于氢氧化钡溶液,沉淀量达最大后,再加氢氧化钡溶液,沉淀量不变,故A错误;
B、由图可知溶解氢氧化铝需要1mol氢氧化钡,由Al(OH)3+OH-=AlO2-+2H2O可知沉淀中Al(OH)3为2mol,故KAl(SO4)2为2mol,加入3mol氢氧化钡,可以生成硫酸钡3mol,n(Al3+):n(OH-)=2mol:6mol=1:3,发生反应Al3++3OH-═Al(OH)3↓,可以得到2molAl(OH)3,沉淀为3mol+2mol=5mol,再加入氢氧化钡,又生成硫酸钡,且氢氧化铝会逐渐溶解,最终沉淀为4mol,故B错误;
C、由图可知溶解氢氧化铝需要1mol氢氧化钡,由Al(OH)3+OH-=AlO2-+2H2O可知沉淀中Al(OH)3为2mol,故Al2(SO4)3为1mol,加入3mol氢氧化钡,可以生成硫酸钡3mol,n(Al3+):n(OH-)=2mol:6mol=1:3,发生反应Al3++3OH-═Al(OH)3↓,可以得到2molAl(OH)3,沉淀为3mol+2mol=5mol,故C正确;
D、偏铝酸钠与氢氧化钡不反应,不能产生沉淀,故D错误;
故选C.
点评 本题以图象为载体考查镁铝化合物的性质,难度中等,明确发生的化学反应是解答的关键,反应发生的先后顺序是学生解答中的难点,注意图象比例关系.


科目:高中化学 来源: 题型:选择题
| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,容器内只含有18O2、S18O2、S18O3分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
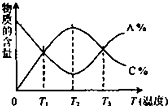 经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )
经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是( )| A. | 该反应在T1、T3温度时达到化学平衡 | |
| B. | 升高温度,平衡会向正反应方向移动 | |
| C. | 该反应的逆反应是放热反应 | |
| D. | 该反应在T2温度时达到化学平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁表面镀锌,锌作阳极 | |
| B. | 船底镶嵌锌块,锌作正极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 工业上电解饱和食盐水的阳极反应:2Cl--2e-═Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与醋酸反应:Zn+2H+═Zn2++H2↑ | |
| B. | 铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Br2+6KOH═5KBr+KBrO3+3H2O | |
| B. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+2H2O+Cl2↑ | |
| C. | 2KNO3 $\frac{\underline{\;\;△\;\;}}{\;}$ 2KNO2+O2↑ | |
| D. | NH4NO3 $\frac{\underline{\;\;△\;\;}}{\;}$ N2O↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com