
| A. | 2KMnO4+H2O2+3H2SO4=K2SO4+2MnSO4+4H2O+3O2↑ | |
| B. | 2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+6H2O+4O2↑ | |
| C. | 2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑ | |
| D. | 2KMnO4+7H2O2+3H2SO4=K2SO4+2MnSO4+10H2O+6O2↑ |
分析 该反应为氧化还原反应,H2O2中氧元素的化合价为-1价,反应后生成0价的氧气,化合价至少升高2价;KMnO4中Mn元素的化合价为+7价,反应后变为+2价的锰离子,化合价降低了5价,化合价变化的最小公倍数为10,然后根据氧化还原反应中化合价变化相等配平即可.
解答 解:H2O2中氧元素的化合价为-1价,反应后生成0价的氧气,化合价至少升高2价;KMnO4中Mn元素的化合价为+7价,反应后变为+2价的锰离子,化合价降低了5价,化合价变化的最小公倍数为10,
氧化还原反应中化合价升降总数一定相等,则H2O2的系数为5,KMnO4的稀系数为2,然后结合质量守恒定律配平可得:2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑,
故选C.
点评 本题考查了化学方程式书写、氧化还原反应的配平,题目难度中等,明确氧化还原反应的配平方法为解答关键,试题培养了学生的分析能力及灵活应用能力.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
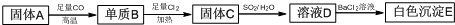
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定新制氯水的pH=2 | |
| B. | 用玻璃棒在过滤器上搅拌以加速硫酸铜晶体的洗涤 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则该溶液中不一定含有SO${\;}_{4}^{2-}$ | |
| D. | 向可溶性淀粉溶液中滴加碘酒,溶液呈蓝色,用CCl4作萃取剂振荡、静置后,下层呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碘化钾溶液中加入浓溴水2I-+Br2═2Br-+I2 | |
| B. | 小苏打与盐酸反应CO32-+2H+═CO2↑+H2O | |
| C. | 氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
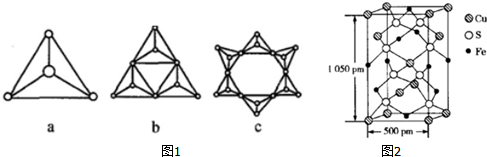
| 物质 | 熔点/℃ | 沸点/℃ | 水溶液 |
| 甲醇 | -97 | 64.7 | 互溶 |
| 甲硫醇 | -123 | 6.8 | 不溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com