
【题目】关于胶体的叙述错误的是
A.溶液显电中性,胶体带有电荷,所以胶体较稳定
B.胶体粒子能透过滤纸,但不能透过半透膜,所以可用渗析的的方法精制胶体
C.可用丁达尔效应区分溶液和胶体
D.电泳实验说明了胶体粒子能吸附溶液中的阳离子或阴离子而带有电荷
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是—种极强的氧化剂,常应用于饮用水处理,其工业制备方法如图所示:
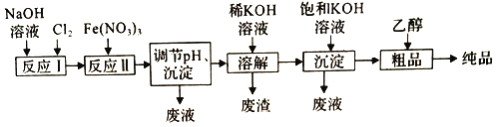
(1)高铁酸钾中铁元素的化合价是__________价。
(2)反应I的目的是________________________________。
(3)反应II的离子方程式为________________________________。
(4)洗涤粗品时选用乙醇而不用水的理由是________________________________。
(5)己知生成高铁酸钾的反应为Na2FeO4+2KOH![]() K2FeO4↓+2NaOH,请你解释加入饱和KOH溶液能生成高铁酸钾的理由是_________________________。
K2FeO4↓+2NaOH,请你解释加入饱和KOH溶液能生成高铁酸钾的理由是_________________________。
(6)为了提高生活用水的卫生标准,自来水厂常使用高铁酸钾(K2FeO4)进行消毒、净化以及改善水质,其消毒原理是______________________。
(7)可用亚铬酸盐滴定法测定高铁酸钾含量,滴定时有关反应的离子方程式为:
①FeO42-+CrO2-+2H2O==CrO42-+Fe(OH)3↓+OH-
②2CrO42-+2H+=CrO72-+H2O
③CrO72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
现称取2.084g高铁酸钾样品溶于适量NaOH溶液中,加入稍过量的NaCrO2,充分反应后过滤,滤液在250mL容量瓶中定容。每次取25.00mL加入稀硫酸酸化,用0.1000mol·L-1的FeSO4标准溶液滴定,三次滴定消耗标准溶液的平均体积为20.00mL。则上述样品中K2FeO4 的质量分数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法正确的是( )
A.1 mol氦气中有2NA个氦原子
B.14 g氮气中含NA个氮原子
C.2 L 0.3 molL﹣1 Na2SO4溶液中含0.6 NA个Na+
D.18 g水中所含的电子数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过石油裂解制得A。以A为原料制取有机玻璃N及隐形眼镜材料M的合成路线如下:
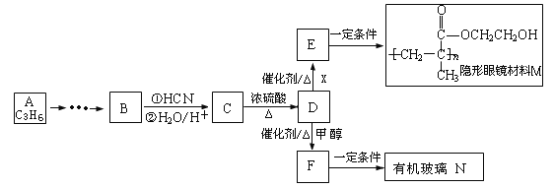
已知: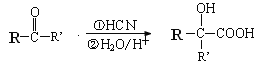 (-R,-R’为可能相同或可能不同的原子或原子团)
(-R,-R’为可能相同或可能不同的原子或原子团)
请回答:
(1)A中官能团的名称是_______,B的结构简式是______。
(2)F→N反应的化学方程式是________,反应类型是________。
(3)C在一定条件下转化为高分子化合物的化学方程式是________。
(4)D有多种同分异构体,符合下列条件的有____种(包括顺反异构体)。
①能发生银镜反应 ②能与NaOH溶液反应
(5)B是一种重要的工业溶剂,请完成A→B的反应的合成路线(有机物写结构简式、无机试剂任选):___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.1molFeCl3与沸水反应生成NA个Fe(OH)3胶粒
B.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl﹣个数为1NA
C.25℃,1.01×105Pa,11.2L Cl2含有的分子数小于0.5NA
D.常温下,23 g NO2含有2NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是无色透明液体,易溶于水、易挥发,见光易分解,具有强氧化性的高效消毒剂,使用过氧乙酸消毒剂时通常先用水稀释工业品过氧乙酸,然后用喷雾法对 空气与地面进行消毒.
(1)配制 220mL0.05mol/L 的过氧乙酸溶液,需使用的仪器有:烧杯、量筒、玻璃棒胶头滴管及
(2)配制过程中,可能引起浓度偏高的操作有 ;
A.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
B.转移溶液时,不慎有少量溶液洒在容量瓶外
C.定容时,俯视容量瓶刻度线进行定容
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,补充几滴水至刻度线
(3)下列叙述正确的是 (填字母)
A.可用过滤的方法将过氧乙酸溶液中混有的 NaCl 除掉
B.过氧乙酸应注意密闭、低温保存于棕色细口瓶中
C.过氧乙酸是一种有机物,它可以用于萃取碘水中的碘单质
(4)过氧乙酸半小时内会完全分解生成乙酸(CH3COOH)和一种常见的气体单质,检验该气体单质的实验方法是
(5)如果生产过氧乙酸的原料 CH3COONa 中混有了 SO42﹣ , 要想除掉 SO42﹣请选择下列试剂按照加入先后顺序填空(试剂不必选完,填序号即可)
①盐酸 ②醋酸钡溶液 ③氯化钡溶液 ④醋酸 ⑤碳酸钠溶液 ⑥碳酸氢钠溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________,表中b_________c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________mol·L-1,0~20s内N2O4的平均反应速率为________________;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________(保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中溶质的物质的量浓度为1mol/L的是( )
A.将40gNaOH溶解在1L水中
B.将1L10mol/L的浓盐酸加入9L水中
C.将22.4LHCl气体溶于水配成1L溶液
D.将10gNaOH溶解在少量水中,再加蒸馏水直到溶液体积为250mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com