
【题目】在密闭容器中充入A2和B2,一定条件下发生反应A2+B2![]() 2AB(正反应为吸热反应),其反应速率与时间的关系如图所示。
2AB(正反应为吸热反应),其反应速率与时间的关系如图所示。

下列说法错误的是( )
A.t1时,v(正反应)>v(逆反应)
B.t2时,v(正反应) = v(逆反应)
C.图中虚线表示的转化是A2+B2→2AB
D.升高温度和加催化剂,均有利于加快反应速率
 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
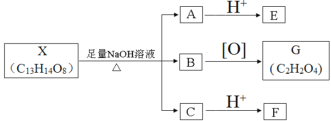
【题目】![]() 是有机物X的结构(其中I、II为未知部分的结构)。
是有机物X的结构(其中I、II为未知部分的结构)。
已知: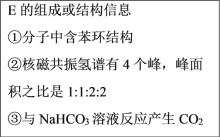
请回答:
(1)E的结构简式_______。
(2)写出B与G反应生成高分子化合物的化学方程式_______。
(3)X的结构简式是_______。
(4)能同时满足下列条件的E的同分异构体共有_______种(不考虑立体异构)。
①能发生银镜反应;②不能发生水解反应;③能与FeCl3溶液发生显色反应。
请写出其中一种核磁共振氢谱为4组峰,且峰值面积比为1∶1∶2∶2的同分异构体的结构简式_______。
(5)F是一种重要的化工原料。
已知:(i)RCH2Br![]() RCH2COOH
RCH2COOH
(ii)RCH2COOH![]() RCH(Cl)COOH
RCH(Cl)COOH
由B经过下列途径可合成F(部分反应条件略):
![]()
N→R的反应类型是_______;
R→T的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】布洛芬具有降温和抑制肺部炎症的双重作用。一种制备布洛芬的合成路线如下:
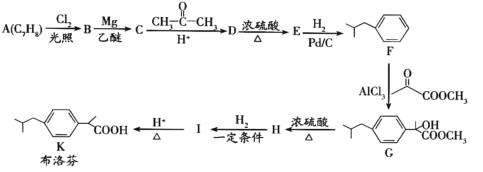
已知:①CH3CH2Cl![]() CH3CH2MgCl
CH3CH2MgCl![]()
![]()
②![]()
![]()
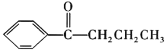 +HCl
+HCl
回答下列问题:
(1)A 的化学名称_____,G→H 的反应类型_____,H 中官能团的名称_________。
(2)分子中所有碳原子可能在同一平面上的 E 的结构简式_____。
(3)I→K 的化学方程式为_____。
(4)写出符合下列条件的 D 的同分异构体的结构简式_____ (不考虑立体异构)。
①能与 FeCl3溶液发生显色反应;
②分子中有一个手性碳原子;
③核磁共振氢谱有七组峰
(5)写出以间二甲苯、CH3COCl 和(CH3)2CHMgCl 为原料制备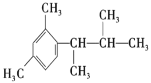 的合成路线________ (无机试剂任选)
的合成路线________ (无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,某一气态平衡体系中含有X、Y、Z、W四种气体物质,此温度下发生反应的平衡常数表达式为:![]() ,有关该平衡体系的说法正确的是( )
,有关该平衡体系的说法正确的是( )
A.升高温度,平衡常数K增大 ,则正反应为吸热反应
B.增大压强,W质量分数增加
C.增大X浓度,平衡向正反应方向移动
D.升高温度,若混合气体的平均相对分子质量变大,则正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以“赏中华诗词、寻文化基因、品生活之美”为基本宗旨的![]() 中国诗词大会
中国诗词大会![]() 不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列诗词分析不正确的是
不仅弘扬了中国传统文化,还蕴含着许多化学知识,下列诗词分析不正确的是![]()
![]()
A.王安石诗句“爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放涉及氧化还原反应
B.诗句“只要功夫深,铁杵磨成针”,该过程只涉及物理变化
C.杜牧诗句“烟笼寒水月笼沙,夜泊秦淮近酒家”,此处的“烟”指固体小颗粒
D.曹植诗句“煮豆燃豆萁,豆在釜中泣”,这里的能量变化主要是化学能转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备锌印刷电路板是用稀硝酸腐蚀锌板,产生的废液称“烂板液”。“烂板液”中除含有硝酸锌外,还含有自来水带入的Cl-和Fe3+。在实验室里用“烂板液”制取znSO4·7H2O的过程如下:
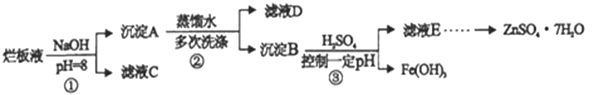
(1)若稀硝酸腐蚀锌板时还原产物为NH4NO3,氧化剂与还原剂的物质的量之比是 _________
(2)若步骤①的pH>12,则Zn(OH)2溶解生成四羟基合锌酸钠,写出Zn(OH)2被溶解的离子方程式_____________
(3)滤液D中除了含有OH-离子外,还含有的阴离子有_________(填离子符号)。
(4)若滤液E的pH=4, c(Zn2+)=2mol/L,c(Fe3+)=2.6×10-9mol/L能求得的溶度积是____(填选项)
A Ksp[Zn(OH)2] B Ksp[Zn(OH)2]和Ksp[Fe(OH)3] C Ksp[Fe(OH)3]
(5)已知:①Fe(OH)3 (s) ![]() Fe3+(aq)+3OH-(aq) △H=a kJ/mol
Fe3+(aq)+3OH-(aq) △H=a kJ/mol
②H2O (l) ![]() H+(aq)+ OH-(aq) △H=b kJ/mol
H+(aq)+ OH-(aq) △H=b kJ/mol
请写出Fe3+发生水解反应的热化学方程式___________
(6)若Fe(OH)3的溶度积常数为Ksp,H2O 的离子积常数为Kw ,Fe3+发生水解反应的平衡常数K=________。(用含Ksp、Kw的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种有机物A的质谱图和红外光谱图如下:
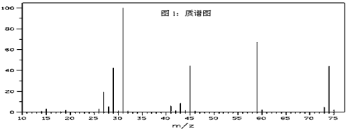
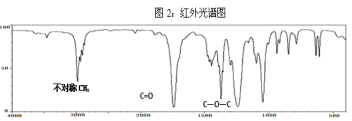
回答下列问题:
(1)结合以上谱图推断:有机物A的相对分子质量为______,分子式为 _____,有机物A的核磁共振氢谱图中有_____种吸收峰,峰面积之比为_______。该有机物与氢氧化钠溶液在加热条件下反应的化学方程式为:_______。
(2)直链烃B的相对分子质量比A小4,含2个甲基,并能使溴的四氯化碳溶液褪色,写出B所有可能的结构简式:______________、__________________。
(3)链烃C是B的同系物,且其对乙烯的相对密度为3,C的核磁共振氢谱显示:C中只含有一种氢原子。则C在一定条件下发生聚合反应的方程式为:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 电解精炼铜时转移了NA个电子,阳极溶解了32g铜
B. 1mol FeCl3完全水解后可生成NA个氢氧化铁胶粒
C. 常温下,1mol氯气通入足量水中发生反应转移的电子数为NA
D. 100mL 0.1mol/L Na2CO3溶液中含有的阴离子数目大于0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1molL-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵。请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)__。
(2)已知T℃,KW=1×10-13,则t℃___25℃(填“>”、“<”或“=”)。在T℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=_。
(3)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与bL该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=__(填数据);
②若x+y>14,则a/b=__(填表达式);
③该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为__(填表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com