
铁及其化合物与生产、生活关系密切。
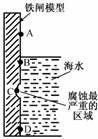
(1)右图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为 。
②图中A和B区域相比较,腐蚀较慢的是 (填字母)。
(2)实验室经常用到FeCl3溶液,在配制FeCl3溶液时常需加入少量 的 ;将FeCl3溶液和碳酸氢钠溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(3)已知t℃时,反应FeO(s)+CO(g) Fe( s) +CO2(g)的平衡常数K= 0.25。
Fe( s) +CO2(g)的平衡常数K= 0.25。
①t℃时,反应达到平衡时n(CO2):n(CO)=
②若在1L密闭容器中加人0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时
FeO(s)转化率为50%,则x= 。
(1) 吸氧腐蚀 A ------------------------------------------------(各1分,共2分)
(2) HCl(或盐酸) ------------------------------------------------------------------------------------(2分)
Fe3++3HCO3-==Fe(OH)3↓+3CO2↑-----------------------------------------------------------------(2分)
(3) 4:1 0.05 ----------------------------------------------------------------------------(各1分)


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
我国“蛟龙”号载人潜水器已成功下潜至海中7020米处。“蛟龙”号载人潜水器的外壳是耐超高压的钛合金,下面有关说法中正确的是
A.钛合金是一种新型金属单质 B.钛合金硬度比成分金属大
C.钛合金的性质与钛单质相同 D.青铜、合金钢和硬铝都是合金
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ/mol,则下列说法中正确的是
A.浓硫酸和稀NaOH溶液反应,生成 l mol水时放热57.3 kJ
B.含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ
C.1L 0.l mol/L CH3COOH与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ
D.1L 0.l mol/L HNO3与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2A(g) 2B(g)+C(g)ΔH<0,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是
2B(g)+C(g)ΔH<0,在未用催化剂的条件下已达平衡,现要使正反应速率降低,c(B)减小,应采取的措施是
A.升温 B.增大反应器的体积 C.增大c(A) D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是
A.Mg2+ + 2HCO3- + 2Ca2+ + 4OH-= Mg(OH)2↓+ 2CaCO3↓+ 2H2O
B.Cu2+ + H2S = CuS↓+ 2H+
C.Zn2+ + S2- + 2H2O = Zn(OH)2↓+ H2S↑
D.FeS + 2H+ = Fe2+ + H2S↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质比较中不正确的是 ( )
A.沸点的高低: B.熔点:SiO2>CsCl>CBr4>CF4
B.熔点:SiO2>CsCl>CBr4>CF4
C.硬度:镁>铝>镁铝合金 D. 水溶性:HF>Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
冰晶胞中水分子的空间排列方式与金刚石晶胞类似,如下图:
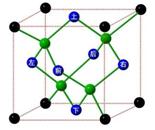
(1)一个水分子含_____个孤电子对,水分子能与很多金属离子形成配合物,请写出它与铜离子形成的一种蓝色的配合物离子的化学式为__________。
(2)每个冰晶胞平均占有____个水分子,冰的熔点远低于金刚石熔点的原因是_____________________。
(3)实验测得冰中氢键的作用力为18.5 kJ/mol,而冰的熔化热为5.0 kJ/mol,这说明冰熔化成水,氢键_____________(填全部或部分)被破坏。
(4)假如冰晶胞边长为a cm,则冰的密度是________________g·cm-3
(阿伏伽德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的熔点高低顺序,正确的是( )
A.金刚石>晶体硅>碳化硅 B.K>Na>Li
C.NaF<NaCl<NaBr D.CI4>CBr4>CCl4>CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。下列有关分析正确的是
A.K3C60中只有离子键 B.C60与12C互为同素异形体
C.该晶体在熔融状态下能导电 D.K3C60中碳元素显-3价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com