
科目:高中化学 来源: 题型:
 (2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:
(2011?上海)实验室制取少量溴乙烷的装置如右图所示.根据题意完成下列填空:| 加热 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
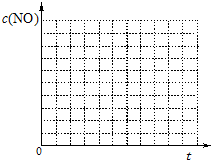
| 时间 | 0 | 1 | 2 | 4 | 4 | 5 |
| c(NO)(×10-4mol?L-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(NO)(×10-3mol?L-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| 实验编号 | T/℃ | NO初始浓度/mol?L-1 | CO初始浓度/mol?L-1 | 催化剂的比 表面积/m2?g-1 |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
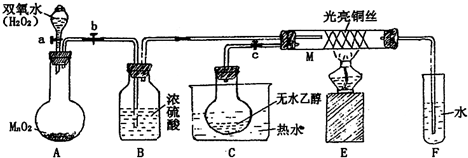
| ||
| ||
| Cu |
| △ |
| Cu |
| △ |
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com