
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
A
解析试题分析:某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子,A.CH3COOH是弱酸,部分电离,在溶液中存在电离平衡:CH3COOH CH3COO-+H+。pH=3,则c(H+)=10-3mol/L.c(CH3COOH)> c(H+)=10-3mol/L;NaOH是强碱,完全电离。pH=11,则c(OH-)=10-3mol/L.若二者等体积混合,则酸已经电离的部分恰好被中和,由于破坏了酸的电离平衡,未电离的酸分子将继续电离,使溶液显酸性。正确。B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成。则二者恰好发生中和反应产生CH3COONa。由于该盐是强碱弱酸盐,弱酸根离子CH3COO-会发生水解反应CH3COO-+H2O
CH3COO-+H+。pH=3,则c(H+)=10-3mol/L.c(CH3COOH)> c(H+)=10-3mol/L;NaOH是强碱,完全电离。pH=11,则c(OH-)=10-3mol/L.若二者等体积混合,则酸已经电离的部分恰好被中和,由于破坏了酸的电离平衡,未电离的酸分子将继续电离,使溶液显酸性。正确。B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成。则二者恰好发生中和反应产生CH3COONa。由于该盐是强碱弱酸盐,弱酸根离子CH3COO-会发生水解反应CH3COO-+H2O CH3COOH+ OH-。当最终达到平衡时c(OH-)> c(H+)。溶液显碱性,与题意不符。错误。C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(H+) >c(OH-)或c(Na+)>c(CH3COO-)>c(OH-)>c(H+),否则违背电荷守恒。错误。D.加入适量氨水,若溶液呈中性c(CH3COO-)等于c(Na+)、c(NH4+)之和,若呈酸性,c(CH3COO-)大于c(Na+)、c(NH4+)之和;若呈碱性,则c(CH3COO-)小于c(Na+)、c(NH4+)之和。错误。
CH3COOH+ OH-。当最终达到平衡时c(OH-)> c(H+)。溶液显碱性,与题意不符。错误。C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(H+) >c(OH-)或c(Na+)>c(CH3COO-)>c(OH-)>c(H+),否则违背电荷守恒。错误。D.加入适量氨水,若溶液呈中性c(CH3COO-)等于c(Na+)、c(NH4+)之和,若呈酸性,c(CH3COO-)大于c(Na+)、c(NH4+)之和;若呈碱性,则c(CH3COO-)小于c(Na+)、c(NH4+)之和。错误。
考点:考查含有相同离子的溶液的配制及离子浓度的大小比较的知识。


科目:高中化学 来源: 题型:单选题
常温下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
| A.加入适量的氢氧化钠固体 | B.将溶液稀释到原体积的 10倍 |
| C.加入等体积0.2 mol·L-1氨水 | D.降低溶液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下,将0.1molAgCl加入1L 0.1mol·L-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是
A.沉淀转化反应2AgCl(s)+ CO32-(aq) Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1 Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1 |
| B.约有2×10-5mol AgCl溶解 |
| C.反应后溶液中的:c(Na+)>c (Cl-) >c (CO32-) >c (OH-) >c (H+) |
| D.反应后溶液中的:c(Na+)+ c (H+)+ c (Ag+)="2" c (CO32-)+ c (HCO3-)+ c (Cl-)+ c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,下列说法正确的是( )
| A.氨水与氯化铵的pH=7的混合溶液中:c(Cl—)>c(NH4+) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—) >c(H2CO3)>c(CO32?) |
| C.pH=12的NaOH溶液与等体积pH=2的醋酸溶液混合后所得溶液显酸性 |
| D.将0.1 mol/L的氨水溶液加水稀释10倍,溶液中离子浓度都减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验操作不能达到其对应目的的是
| 序号 | 实验内容 | 实验目的 |
| A. | 向盛有10滴0.1 mol/L AgNO3溶液的试管中滴加0.1 mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| B. | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C. | 向Na2SiO3溶液中通入CO2 | 证明碳酸的酸性比硅酸强 |
| D. | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 | 验证淀粉已水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法中正确的是
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法中正确的是
①用物质A 表示的反应的平均速率为0.3 mol·L-1·S-1
②用物质B 表示的反应的平均速率为0.6 mol·L-1·S-1
③2 s 时物质A 的转化率为70%
④2 s 时物质B 的浓度为0.7 mol·L-1,
| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在25 ℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24。下列有关说法中正确的是
| A.25 ℃时,CuS的溶解度大于ZnS的溶解度 |
| B.25 ℃时,饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1 |
| C.向物质的量浓度相同的FeCl2、ZnCl2的混合液中加入少量Na2S,只有FeS沉淀生成 |
| D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 |
| B.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 |
C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(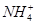 )/c(NH3·H2O)的值增大 )/c(NH3·H2O)的值增大 |
| D.室温下,CH3COOH的KW=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com