
| A. | 1L 0.1mol/L的NaOH溶液中氧原子个数为0.1NA | |
| B. | 3g SiO2中Si-O数目为0.1NA | |
| C. | 0.1 mol钠与足量O2充分反应时,转移的电子数为0.1NA | |
| D. | 0.2 mol SO2与0.1mol O2充分反应,产物的分子数为0.1NA |
分析 A.氢氧化钠溶液中,氢氧化钠和水都含有氧原子;
B.1molSiO2晶体存在4molSi-O键;
C.钠与氧气反应生成+1价钠离子;
D.二氧化硫与氧气反应生成三氧化硫为可逆反应,不能进行到底.
解答 解:A.氢氧化钠溶液中,氢氧化钠和水都含有氧原子,所以1L 0.1mol/L的NaOH溶液中氧原子个数远远大于0.1NA,故A错误;
B.3g SiO2物质的量为$\frac{3g}{60g/mol}$=0.05mol,含有Si-O物质的量为0.05mol×4=0.2mol,即0.2NA,故B错误;
C.0.1 mol钠与足量O2充分反应时,生成0.1mol钠离子,转移的电子数为0.1NA,故C正确;
D.0.2 mol SO2与0.1mol O2充分反应,生成的三氧化硫物质的量小于0.1mol,产物的分子数小于0.1NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,熟练掌握公式的使用和物质的结构是解题关键,注意可逆反应不能进行到底特点,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥ | B. | 只有①② | C. | ①②④ | D. | 只有 ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| B. | 某古剑“以剂钢为刃,铁为茎干,…,”“剂钢”指的是铁的合金 | |
| C. | 《梦溪笔谈》载:“高奴县出脂水,燃之如麻,但烟甚浓”,所述“脂水”属于石油 | |
| D. | 《肘后备急方》载:“青蒿一握,以水二升渍,绞取汁”,如此提取青蒿素纯属萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.30mol/l | B. | 0.225mol/l | C. | 0.45mol/l | D. | 0.36mol/l |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
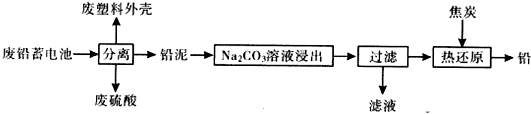
| 物质 | Ksp(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.4×10-20 | 白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
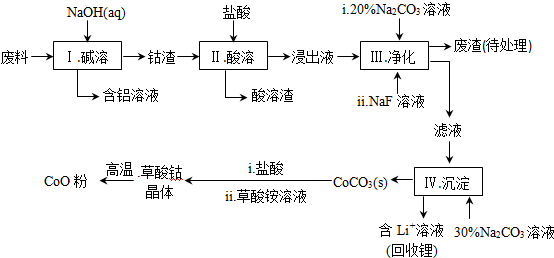
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
 LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去铁粉中的铜粉,加入足量浓硫酸加热反应后进行过滤 | |
| B. | 不用任何其他试剂就可以鉴别NaOH溶液和Al2(SO4)3溶液 | |
| C. | 制备Fe(OH)3胶体时,通常是将Fe(OH)3固体溶于沸水中 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=v逆(H2O) | |
| C. | 容器内混合气体密度保持不变 | |
| D. | 3molH-H键断裂同时断裂3molH-O键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com