
| A、浓盐酸具有还原性 | B、浓盐酸具有挥发性 | C、浓H2SO4具有吸水性 | D、气体溶质的溶解度随温度升高而降低 |


科目:高中化学 来源: 题型:阅读理解
 AgOH+H+
AgOH+H+ AgOH+H+
AgOH+H+
| ||
| ||

 门上的固体材料R可以采用
门上的固体材料R可以采用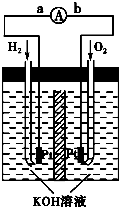 方向为
方向为查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | 溶液变红色 溶液变红色 |
固体物质中FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含 FeCl2 FeCl2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
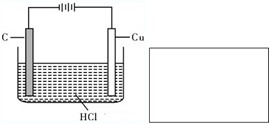 盐酸、硫酸和硝酸是中学常见的三种酸.
盐酸、硫酸和硝酸是中学常见的三种酸.
| ||
| ||

| ||
查看答案和解析>>
科目:高中化学 来源:广东省佛山一中2011-2012学年高二上学期期中考试化学理科试题 题型:013
|
强酸与强碱的稀溶液发生中和反应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,分别向1 L 0.5 mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀盐酸;③稀硝酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是 | |
| [ ] | |
A. |
ΔH1<ΔH2=ΔH3 |
B. |
ΔH1<ΔH2<ΔH3 |
C. |
ΔH1>ΔH2>ΔH3 |
D. |
ΔH1=ΔH2<ΔH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用锌粒与VmL浓度为10%的稀硫酸反应制取氢气,若向反应混合物中加入下列物质,关于反应速率v说法正确的是
A.少量BaCl2固体,v(H2)减小 B.VmLNa2SO4溶液,v(H2)不变
C.VmL浓盐酸,v(H2)增大 D.VmL稀硝酸,v(H2)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com