
某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究。
[探究目的]
分析黑色粉末X的组成,并进行相关实验。
[查阅资料]
①CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。
②Fe3O4+8H+=2Fe3++Fe2++4H2O
③Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
8Fe+30HNO3(更稀)=8Fe(NO3)3+3NH4NO3+9H2O
④3Fe3O4+28HNO3(稀)=9Fe(NO3)3+NO↑+14H2O
[实验探究]
I.定性检验
| 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色;有气泡产生 |
| ② | 向试管1中滴加几滴KSCN溶液,振荡 | 溶液出现血红色 |
| ③ | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
⑴实验③发生的反应的离子方程式为 。
⑵上述实验说明黑色粉末X中含有 。
II.定量测定
根据下图所示的实验方案进行实验并记录数据:
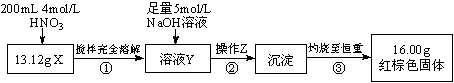
⑴操作Z的名称是 。
⑵通过以上数据,得出13.12g黑色粉末X中各成分的物质的量为 。
[交流讨论]
在实验过程中,发现在溶液Y中滴加过量NaOH溶液时有刺激性气味气体生成。为了确定溶液Y中各离子浓度,甲同学重复上述实验。在步骤①中共收集到标准状况下896mL的气体,经分析其中只含有NO;测得溶液Y中c(H+)=0.5mol/L。
通过计算可知,溶液Y中c(Fe3+)= mol/L,c(NH4+)= mol/L,c(NO3-)= mol/L。
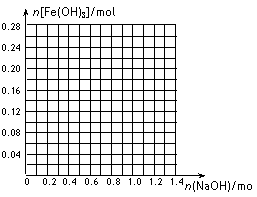 请画出在200mL溶液Y中加入NaOH物质的量与生成的Fe(OH)3沉淀物质的量的关系曲线。
请画出在200mL溶液Y中加入NaOH物质的量与生成的Fe(OH)3沉淀物质的量的关系曲线。
科目:高中化学 来源: 题型:
 某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2011?泰州一模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
(2011?泰州一模)某化学研究性学习小组为探究某品牌花生油中不饱和脂肪酸的含量,进行了如下实验:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com