

分析 无色溶液中不存在有色的Fe3+,加过量盐酸生成气体和溶液,则溶液中一定含CO32-,一定不含有与碳酸根离子反应的Ba2+、Al3+,气体A为CO2;溶液I加入过量氢氧化钡反应生成气体B为氨气,白色沉淀甲是硫酸钡,据此进行解答.
解答 解:无色溶液,判断Fe3+不存在,加过量盐酸生成气体和溶液,判断溶液中一定含CO32-;则一定不含有Ba2+、Al3+;气体A为CO2;溶液I加入过量氢氧化钡反应生成气体B为氨气,一定有铵根离子,白色沉淀甲是硫酸钡,原溶液一定含有硫酸根.
(1)根据分析可知,白色沉淀甲是BaSO4,
故答案为:BaSO4;
(2)碳酸钠溶液与过量稀盐酸混合完全反应生成CO2,反应的离子方程式为CO32-+2H+=H2O+CO2↑,铵盐能与碱反应生成氨气:NH+4+OH-=NH3↑+H2O,
故答案为:CO32-+2H+=H2O+CO2↑;NH+4+OH-=NH3↑+H2O;
(3)X溶液中一定存在的离子是NH4+、CO32-、SO42-,则含有的阴离子为CO32-、SO42-;一定不存在的离子是Fe3+、Ba2+、Al3+,尚未确定是否存在的离子是K+,
故答案为:CO32-、SO42-;K+;
(4)先加入氯化钡溶液生成碳酸钡沉淀,然后用盐酸溶解沉淀,并用澄清石灰水检验生成的气体为二氧化碳,所以检验方法为:取少量待测液于试管中,加入氯化钡溶液有白色沉淀产生,再加足量盐酸,沉淀消失,产生无色无味气体,且该气体能使澄清石灰水变浑浊,
故答案为:取少量待测液于试管中,加入氯化钡溶液有白色沉淀产生,再加足量盐酸,沉淀消失,产生无色无味气体,且该气体能使澄清石灰水变浑浊.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,试题综合性较强,充分培养了学生的分析、理解能力及逻辑推理能力


科目:高中化学 来源: 题型:多选题
| A. | 在含等物质的量的CO32-、OH-的溶液中逐滴加入稀盐酸:OH-、CO32-、HCO3- | |
| B. | 在含等物质的量的Al3+、NH4+的溶液中逐滴加入稀烧碱:Al3+、Al(OH)3、NH4+ | |
| C. | 在含铁和铜的混合物中逐滴加入稀硝酸:Fe、Cu、Fe2+ | |
| D. | 惰性电极电解含等物质的量的Zn2+、Al3+溶液时阴极电极反应:Zn2+、Al3+、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食物溶于水后的溶液pH<7,则为酸性食物 | |
| B. | 由C、H、O、N、S、P等元素组成的蛋白质是酸性食物 | |
| C. | 蔬菜、水果多含钾、钠、钙、镁等盐类及果酸,习惯称为酸性食物 | |
| D. | 柠檬是酸性食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀硫酸存在的条件下可以和2mol乙醇发生酯化反应 | |
| B. | 1mol该有机物与足量金属Na反应生成生成3molH2 | |
| C. | 1mol该有机物最多可与2molNaOH溶液发生反应 | |
| D. | HOOCCH2CH2CH(OH)CH2COOH与该有机物互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
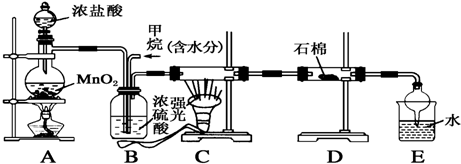
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO为氧化剂,反应过程中被还原 | |
| B. | K2FeO4是还原产物 | |
| C. | K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 | |
| D. | 若有2 mol FeCl3 发生反应,转移电子的物质的量为 6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com