
| 离子半径 | 酸性 |
| Na+< O2- | H2SO4<HClO4 |
分析 (1)S原子核外电子排布式为1s22s22p63s23p4,3p能级中有2个未成对电子;Cu原子核外电子数为29,根据能量最低原理书写核外电子排布式;
(2)电子层结构相同的离子,核电荷数越大离子半径越小;
非金属性越强,最高价含氧酸的酸性越强;
(3)发生反应:4CuCl+O2=2CuO+2CuCl2,计算4molCuCl反应放出的热量,注明物质聚集状态与反应热书写热化学方程式.
解答 解:(1)S原子核外电子排布式为1s22s22p63s23p4,3p能级中有2个未成对电子;Cu原子核外电子数为29,根据能量最低原理,其核外电子排布式为:1s22s22p63s23p63d104s1,
故答案为:2;1s22s22p63s23p63d104s1;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:Na+<O2-;
非金属性S<Cl非金属性越强,最高价含氧酸的酸性越强,故酸性:H2SO4<HClO4,
故答案为:<;<;
(3)发生反应:4CuCl+O2=2CuO+2CuCl2,4molCuCl反应放出的热量为44.4kJ×4=177.6kJ,反应热化学方程式为:4CuCl(s)+O2(g)=2CuO(s)+2CuCl2(s)△H=-177.6kJ/mol,
故答案为:4CuCl(s)+O2(g)=2CuO(s)+2CuCl2(s)△H=-177.6kJ/mol.
点评 本题考查核外电子排布、微粒半径比较、元素周期律应用、热化学方程式书写,比较基础,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 胶体粒子可以通过半透膜而溶液不行,故可以用半透膜来分离胶体和溶液 | |
| C. | 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 | |
| D. | 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 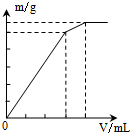 Al2(SO4)2 | B. | 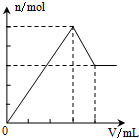 KAl(SO4)2 | C. | 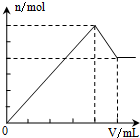 NH4Al(SO4)2 | D. | 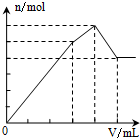 NH4Al(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用含磷洗涤剂 | B. | 用工业污水直接灌溉农田 | ||
| C. | 用O3替代Cl2作饮用水消毒剂 | D. | 含Hg2+的废水直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①③④ | C. | ①② | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
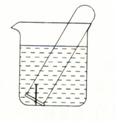 图所示水槽中的试管内有一枚铁钉(含少量的炭),放置数天后观察:
图所示水槽中的试管内有一枚铁钉(含少量的炭),放置数天后观察:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是一种国际基本物理量 | |
| B. | 1 mol氢的质量为1g | |
| C. | 在同温同压下,相同体积的任何气体单质所含分子数相同 | |
| D. | 标准状况下气体摩尔体积约为22.4 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com