
分析 (1)该有机物的摩尔质量为$\frac{3g}{0.5mol}$=60g/mol,计算有机物、水、二氧化碳物质的量,根据质量守恒计算式有机物中氧原子物质的量,根据原子数目之比确定有机物最简式,最后根据相对分子质量求出分子式;
(2)此有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,结合分子式判断含有的官能团,确定其结构简式.
解答 解:(1)该有机物的摩尔质量为$\frac{3g}{0.5mol}$=60g/mol,
12g有机物的物质的量=$\frac{12g}{60g/mol}$=0.2mol,
7.2gH2O中H原子的物质的量为:$\frac{7.2g}{18g/mol}$×2=0.8mol,
标况下8.96LCO2的物质的量为:$\frac{8.96L}{22.4L/mol}$=0.4mol,则n(C)=0.4mol,
12g有机物中:m(C)+m(H)=0.4mol×12g/mol+0.8mol×1g/mol=5.6g,根据质量守恒可知,有机物中含有氧原子的质量为:m(O)=12g-5.6g=6.4g,
则氧原子的物质的量为:n(O)=$\frac{6.4g}{16g/mol}$=0.4mol,
所以:n(C):n(H):n(O)=0.4mol:0.8mol:0.4mol=1:2:1,
该有机物的最简式为:CH2O,分子式为(CH2O)n,又因相对分子质量为60,即:30n=60,解得:n=2.
所以该有机物的分子式为:C2H4O2,
故答案为:C2H4O2;
(2)有机物分子式为C2H4O2,具有弱酸性,能与金属钠反应,也能与碱溶液反应,含有-COOH,结构简式为:CH3COOH,能与NaHCO3溶液反应,反应方程式为:CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O,
故答案为:CH3COOH;能;CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O.
点评 本题考查有机物分子式与结构式的确定,题目难度中等,掌握利用原子守恒确定有机物分子式的方法,注意掌握官能团的结构与性质的关系.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | -867kJ•mol-1 | B. | -574kJ•mol-1 | C. | -691.2kJ•mol-1 | D. | -925.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色 | |
| B. | 浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊 | |
| C. | 将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅 |
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上适应性考试二化学试卷(解析版) 题型:推断题
[化学—选修5:有机化学基础]
化合物X是一种香料,按图所示的路线合成,请回答:

已知: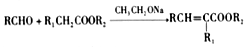
(1).烃A的结构简式是_______________,生成B的反应类型是_______________。
(2).F中所含官能团的名称是____________,已知F能与新制Cu(OH)2悬浊液反应,请写出化学方程式:____________________。
(3).D→E的反应类型是_________,E+C→G的化学方程式:___________________。
(4).对于化合物X,下列说法正确的是___________(填序号)。
A.0.1molX充分燃烧约消耗224L空气(标况)
B.X苯环上的一氯代物有三种
C.X可使Br2的CCl4溶液和KmnO4(H+)溶液褪色,且原理相同
D.X在酸性条件下的水解产物均可与C2H5OH反应
⑸.与G含有相同官能团,且苯环上只有一个取代基的同分异构体有____________种,W为其中一种,具有下列结构特征:A.能发生银镜反应,B.核磁共振氢谱显示有五组峰,峰面积之比为6:2:2:1:1。写出W的结构简式:_____________________。
⑹.以甲苯和乙烯为起始原料,选用必要的无机试剂合成二苯甲酸乙二酯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上适应性考试二化学试卷(解析版) 题型:选择题
固体粉未X可能含有Fe、Fe3O4、CuO、MnO2、Na2SO4和NaSO3中的若干种,为确定该固体粉末的成分,某同学依次进行了以下实验:①将X加人足量水中,得到不溶物Y和溶液Z;②取少量Y加人足最浓盐酸,加热,产生黄绿色气体.并有少量红色不溶物;③向Z溶液中滴加BaCl2溶液,生成白色沉淀,再加足量稀硝酸沉淀不溶解。分析以上实验现象,下列结论正确的是
A.X中一定不存在Fe3O4
R.Y中不一定存在MnO2
C.Z溶液中一定含有Na2SO4
D.不溶物Y中一定含有Fe和CuO
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
有关下列说法的判断正确的是
A. 漂白粉在空气中不稳定,可用于漂白纸张
B. 漂白粉中的CaCl2与空气中的CO2反应可生成CaCO3,漂白粉在空气中久置变质
C.NH3能使酚酞溶液变红,因而NH3可用于设计喷泉实验
D. 打磨磁石制指南针不涉及化学反应
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上学期期中化学试卷(解析版) 题型:实验题
高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制480mL 0.1000 mol·L-1的酸性KMnO4溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、 。用天平需要称量固体KMnO4的质量 。
②下列操作导致所配制溶液的浓度偏大的是 (填序号)。
a.加水定容时俯视刻度线 b.容量瓶底部有少量蒸馏水
c.颠倒摇匀后发现凹液面低于刻度线又加水补上 d.天平的砝码生锈
(2)某化学兴趣小组利用滴定的方法,用新配制的酸性KMnO4溶液来测定某试剂厂生产的FeSO4溶液中Fe2+的物质的量浓度。
①酸性高锰酸钾溶液与FeSO4溶液反应的离子方程式为 。
②该小组在测定过程中发现,测得的Fe2+的物质的量浓度比标签上的标注值要低,在滴定操作准确的前提下,可能导致该测定结果的原因如下:
猜想一:FeSO4溶液变质;证明方法是 ;
猜想二: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com