
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:解答题
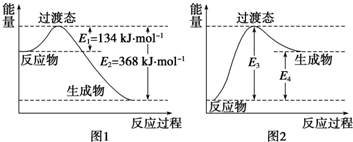
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石比石墨稳定 | |
| B. | 1mol 石墨比1mol金刚石的总能量高 | |
| C. | 金刚石和石墨互为同位素 | |
| D. | 石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,但不能直接与水反应生成H2SiO3 | |
| B. | N2是大气中的主要成分之一,雷雨时可直接转化为NO2 | |
| C. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{34}^{78}$ Se 和${\;}_{34}^{80}$Se所含电子数不同 | |
| B. | ${\;}_{34}^{78}$Se和 ${\;}_{34}^{80}$Se都含有34个中子 | |
| C. | ${\;}_{34}^{78}$ Se和${\;}_{34}^{80}$ Se 分别含有44和46个质 | |
| D. | ${\;}_{34}^{78}$ Se和${\;}_{34}^{80}$Se互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 两极材料 | Zn片、石墨 | Cu片、Fe片 | Fe片、石墨 | Fe片、Cu片 |
| 插入溶液 | 稀硫酸 | 浓 HNO3 | FeCl3溶液 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二次模拟化学试卷(解析版) 题型:选择题
取100mL 18.3mol•L﹣1 的H2SO4与Zn反应,当Zn完全溶解时,生成的气体(可使品红褪色)在标准状况下的体积为22.4L.将所得的溶液稀释成1L,测得溶液H+的浓度为1mol•L﹣1,则所生成的气体中SO2与H2的体积比约为( )
A.1:2 B.2:1 C.1:4 D.4:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com