
��11�֣�
��1����һ�ܱյ�2 L�����������8 mol SO2��4 mol18O2����һ�������¿�ʼ��Ӧ��
2SO2��g����O2��g�� 2SO3��g��2 minĩ�����������7.2 mol SO2���Իش�
2SO3��g��2 minĩ�����������7.2 mol SO2���Իش�
�ٷ�Ӧ��18Oԭ�Ӵ�������Щ������________
��2 minĩSO3��Ũ��Ϊ________
����O2��Ũ�ȱ仯��ʾ��ʱ����ڵĻ�ѧ��Ӧ����Ϊ________
��2����������ԭ�ϱ�����ϩ��������ʮ�ֹ㷺����;����ش�
�ٿ�������������������ϩ���Լ���________������ţ�
A��ˮ B��������Ȼ�̼��Һ C�����Ը��������Һ D������
�ڱ����Ӿ���ƽ���������νṹ������ԭ�ӹ�ƽ�棬��������һ��ֱ���ϵ�ԭ�������________��
��3������Ӫ�������������ڷ����ı仯������˵��������������ò���ȷ����
A�������е����ࡢ��֬�͵����ʶ���Ϊ�˵�������ṩ����
B�����ۺ���ά�� ������
������  CO2��H2O(�ͷ�����ά���������
CO2��H2O(�ͷ�����ά���������
C����֬  ���ͺ�֬����
���ͺ�֬���� CO2��H2O(�ͷ�����ά���������
CO2��H2O(�ͷ�����ά���������
D�������� ������
������ ��������ĵ����ʣ����������������³´�л��
��������ĵ����ʣ����������������³´�л��
��11�֣�
��1���� SO2 O2 SO3 ��1�֣�
�� 0.4 mol/L ����λ��д��1�֣� ��2�֣�
�� 0.1 mol/(L?min) ����λ��д��1�֣� ��2�֣�
��2���� BC ��2�֣�
�� 4 ��2�֣�
��3�� B ��2�֣�
��������
�����������1���ٸ÷�ӦΪ���淴Ӧ��SO2�л���18Oԭ��
��2 minĩ�����������7.2 mol SO2��0.8 mol SO2ת����0.8 mol SO3��Ũ��Ϊ0.4 mol/L
��2 min 0.8 mol SO2ת����0.8 mol SO3��0.4 mol O2 ת�������������ݻ�������ʱ�䣬�õ�
0.1 mol/(L?min)
��2�������Ը��������Һ ��ʹ���Ը��������Һ��ɫ������ϩ���ֲ����״�����ϲ���DZ�����״�����²�������Ȼ�̼ ����ˮ�����Ȼ�̼��Һ ��ʹ��ˮ��ɫ������ϩ���ֲ���²���ɫ�������Ȼ�̼���ϲ���ɫ���DZ���
���㣺��ѧ��Ӧ�����뻯ѧƽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014������Ͽ���������ģ�Ծ����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��18�֣��ס��������о���ѧϰС��Ϊ�ⶨ�������е�����ԭ�Ӹ����ȣ����������ʵ�����̣�
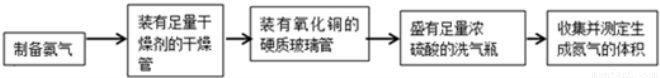
ʵ���У������Ƶõİ����ž�ϴ��ƿǰ����װ���еĿ�����������ϴ��ƿ�������ռ�װ �ã�������������ͭ����Ӧ��ɺ�ɫ����ͭת��Ϊ��ɫ��ͭ����ͼA��B��CΪ�ס�����С����ȡ����ʱ�����õ���װ�ã�DΪʢ��Ũ�����ϴ��ƿ��
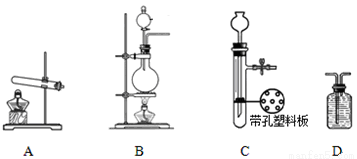
��С���ã���Ӧǰ����ͭ������m1 g������ͭ��Ӧ��ʣ����������m2g�����ɵ����ڱ�״���µ����V1L����С���ã�ϴ��ǰװ��D������m3g��ϴ����װ��D������Ϊm4g�����ɵ����ڱ�״���µ����V2L����ش��������⣺
��1�����Aװ�������ԵIJ�����____________________________________________________��
��2��ʵ���Ҽ��鰱���IJ�����������____________________________________��
��3���ס�����С��ѡ���˲�ͬ�ķ�����ȡ�������뽫ʵ��װ�õ���ĸ��ź��Ʊ��Ʊ�ԭ����д���±��Ŀո��С�
| ʵ��װ�� | ʵ��ҩƷ | �Ʊ�ԭ�� |
��С�� | A | �������ơ������ | ��Ӧ�Ļ�ѧ����ʽΪ____________ |
��С�� | _____ | Ũ��ˮ���������� | �û�ѧƽ��ԭ�������������Ƶ����ã�_______ |
��4����С�����������ݼ�����������е������ԭ�Ӹ���֮��Ϊ________________��
��5����С�����������ݼ�����������е������ԭ�Ӹ���֮������С������ֵ����ԭ����_______��Ϊ�ˣ���С����ԭ��ʵ��Ļ�����������һ��װ��ijҩ����ʵ������������ʵ�顣����ʵ��ǰ���ҩƷ�������仯�����ɵ�����������ó��˺�����ʵ��������ҩƷ��������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ж�������һѧ����ĩ��������һ�꼶��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ڵ���ʵ���
A���������� B��ͭ C������ D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и����е������л�������ʽ��ͬ���Ȳ���ͬϵ��ֲ���ͬ���칹�����
A���� ����ϩ B����ȩ �Ҷ�ȩ
C���Լ����� ���״� D������ ��ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��Ӧ��û����ɫ�仯����
A������FeCl3 ��Һ ����������������B���������ˮ
C������K2Cr2O7��Һ��C2H5OH ���� D��C3H7Cl��NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ظ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭ�Ĺ����з���:Cu2S + 2Cu2O = 6Cu + SO2��,������������ȷ����
A���÷�Ӧ�ӵ���ת�ƽǶȿ�����SO2 + 2H2S = 3S + 2H2O��ͬһ��Ӧ����
B���÷�Ӧ�ӵ���ת�ƽǶȿ���ÿ����6 molͭ��ת�Ƶ���12 mol
C���÷�Ӧ�У���Ԫ����������Ԫ��
D���÷�Ӧ�У�Cu2S���ǻ�ԭ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ظ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʲ���ʹ���Ը��������Һ��ɫ����
A����������B����
C����ϩD���Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�Ĵ�������ѧʵ��ѧУ�߿�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ�����õ绯ѧ���ⷨ����ˮ�е���������Ⱦ�������м������ӽ���Ĥ��������ˮ����II����ͨ��ʹתNO3����ΪN2������˵������ȷ���� �� ��

A�����ʱH+��I��ͨ�����ӽ���ĤǨ�Ƶ�II��
B��Ag-Pt�缫�Ϸ�����Ӧ��2 NO3��+10e��+6H2O= N2��+12OH��
C������������ת����1moL���ӣ���II�����Һ��������2.8g
D��Ϊ��ǿ��Һ�ĵ����ԣ�I��ˮ�пɼ�������Na2SO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�Ĵ�ʡ��ѧ�����п��Ը߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ӣ�Ni��Cd���ɳ�������ִ��������й㷺Ӧ�ã����ij�ŵ練Ӧ����ʽ���У�
Cd(OH)2+2Ni(OH)2  Cd+2NiO(OH)+2H2O �ɴ˿�֪���õ�طŵ�ʱ�ĸ��������� �� ��
Cd+2NiO(OH)+2H2O �ɴ˿�֪���õ�طŵ�ʱ�ĸ��������� �� ��
A��Cd(OH)2 B��Ni(OH)2 C��Cd D��NiO(OH)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com