
 |  |  |  | |||||||||
| 化工 | 氯碱工业 | 高炉炼铁 | 铜的精炼 | 生产漂白粉 | ||||||||
| 原理 | 2H2O+2NaCl
| 3CO+Fe2O3
| 阴极: Cu-2e-═Cu2+ | 2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O | ||||||||
| A | B | C | D |
| A、A | B、B | C、C | D、D |


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
 鸦片最早用于药物(有止痛、止泻、止咳的作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如右.该物质在一定条件下与Br2发生苯环上取代反应生成的一溴代物的同分异构体的种数分别为( )
鸦片最早用于药物(有止痛、止泻、止咳的作用),长期服用会成瘾,使人体质衰弱,精神颓废,寿命缩短.鸦片具有复杂的组成,其中的罂粟碱的分子结构如右.该物质在一定条件下与Br2发生苯环上取代反应生成的一溴代物的同分异构体的种数分别为( )| A、5 | B、6 | C、7 | D、8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是元素周期表短周期元素的一部分.已知M最高价氧化物对应的水化物为常见的氧化性酸,下列说法正确的是( )
如图是元素周期表短周期元素的一部分.已知M最高价氧化物对应的水化物为常见的氧化性酸,下列说法正确的是( )| A、M为氮元素 |
| B、原子半径:Y>X |
| C、氢化物沸点:X>N |
| D、M、X、Y三种元素的最高价氧化物对应的水化物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
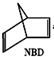
| 太阳光 |
| 暗处 |
 △H=+88.62kJ/mol下列有关说法不正确的是( )
△H=+88.62kJ/mol下列有关说法不正确的是( )| A、等质量的NBD和Q,物质Q具有的总能量比NBD的低 |
| B、一定条件下,1 mol NBD最多可与2 mol Br2发生加成反应 |
| C、物质Q的一氯取代物只有3种 |
| D、NBD和Q二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂 |
| B、升高温度 |
| C、充入N2 |
| D、增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有酸性,没有碱性 |
| B、只有碱性,没有酸性 |
| C、既有酸性,又有碱性 |
| D、既没有酸性,又没有碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y→乙醛属于消去反应 |
| B、X可以是淀粉或纤维素 |
| C、Y与CH3OCH3是同分异构体 |
| D、Y可以用于消除少量钠屑 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com