
| A. | C3H6 | B. | C6H6 | C. | C4H10 | D. | C4H8 |
科目:高中化学 来源: 题型:选择题
| A. | 制钛:用金属钠在高温下氧化TiCl4 | |
| B. | 炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物 | |
| C. | 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 | |
| D. | 制镁:用海水为原料,经一系列过程制得氧化镁固体,用氢气还原氧化镁得到镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的充、放电过程互为可逆反应 | |
| B. | 放电时,电池的负极反应为 Li-e-═Li+ | |
| C. | 放电过程中,Li+向电池的负极移动 | |
| D. | 该电池可以采用醋酸、乙醇等作为电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有18个纵行,每一个纵行是一族 | |
| B. | 34号元素位于第四周期VA族 | |
| C. | 只有一种元素组成的物质一定是纯净物 | |
| D. | 同素异形体之间的相互转化属于化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol S和O2的摩尔质量都是32 g | |
| B. | 7.8g Na2S与Na2O2的混合物约含有阴离子6.02×1022个 | |
| C. | 1mol任何气体中都含有相同的原子数 | |
| D. | 22.4LCO2气体中含有3NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离产生的c(OH-)=10-13mol/L的溶液:Al3+、Na+、Cl- | |
| B. | 使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、SO42- | |
| C. | 0.1 mol/L AlCl3的溶液:NH4+、AlO2-、ClO- | |
| D. | 0.1 mol/L FeCl3溶液:K+、Br-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
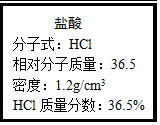 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8克Na2O2加入100克水中所得溶液中含氧原子0.2NA个 | |
| B. | 标准状况下,11.2LCCl4中含2NA个σ键 | |
| C. | 用惰性电极电解氯化铜溶液,当阳极产生标准状况下黄绿色气体6.72L时,则电路中转移的电子数为0.6NA | |
| D. | 将20.00mL1.5mol/LFeCl3溶液制成胶体,则所得胶体中含有0.03NA个胶粒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com