
下列离子方程式正确的是( )
|
| A. | 向CuSO4溶液中投入Na:Cu2++2Na═Cu+2Na+ |
|
| B. | 向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN﹣═Fe(SCN)3↓ |
|
| C. | 向NaHCO3溶液中加过量Ca(OH)2溶液:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O |
|
| D. | 向BaCO3固体中加入过量的稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |
| 离子方程式的书写. | |
| 专题: | 离子反应专题. |
| 分析: | A.活泼金属钠和盐的反应是和盐中的水反应; B.Fe(SCN)3是溶液; C.少量碳酸氢钠与氢氧化钙反应生成碳酸钙; D.硫酸钡是白色沉淀. |
| 解答: | 解:A.活泼金属钠和盐的反应一定是先和盐中的水反应,不会置换出其中的金属:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4,故A错误; B.Fe(SCN)3是溶液,不是沉淀,故B错误; C.少量碳酸氢钠与过氢氧化钙完全反应生成碳酸钙:Ca2++HCO3﹣+OH﹣═CaCO3↓+H2O,故C正确; D.反应生成硫酸钡是白色沉淀,覆盖在碳酸钙表面,阻止反应进一步进行,离子方程式:BaCO3+2H++SO42﹣═BaSO4+CO2↑+H2O,故D错误. 故选:C. |
| 点评: | 本题考查离子方程式的书写,题目难度中等,本题中注意把握物质的性质以及反应的过量问题,C为易错点. |


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
关于晶体的下列说法正确的是( )
A.化学键都具有饱和性和方向性
B.晶体中只要有阴离子,就一定有阳离子
C.氢键具有方向性和饱和性,也属于一种化学键
D.金属键由于无法描述其键长、键角,故不属于化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
酸雨是因为过度燃烧煤和石油,生成硫的氧化物及氮的氧化物溶于水而生成硫酸和硝酸的缘故。某次雨水的分析数据如下:
c(NH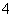 )=2.0×10-5 mol·L-1,c(Cl-)=6.0×10-5 mol·L-1,c(Na+)=1.9×10-5 mol·L-1,
)=2.0×10-5 mol·L-1,c(Cl-)=6.0×10-5 mol·L-1,c(Na+)=1.9×10-5 mol·L-1,
c(NO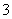 )=2.3×10-5 mol·L-1,c(SO
)=2.3×10-5 mol·L-1,c(SO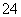 )=2.8×10-5 mol·L-1。
)=2.8×10-5 mol·L-1。
则该酸雨的pH为( )
A.5.6 B.4.3
C.5 D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
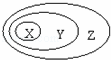
下表中所示物质或概念间的从属关系符合如图的是
|
| X | Y | Z |
| A | 钠元素 | 主族元素 | 短周期元素 |
| B | 电解质 | 化合物 | 纯净物 |
| C | 氢氧化铁 | 胶体 | 分散系 |
| D | 置换反应 | 氧化还原反应 | 放热反应 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是某研究性学习小组对离子方程式 xR2++yH++O2═mR3++nH2O的分析研究.在下面的各种说法中错误的是( )
|
| A. | 可以根据电荷守恒,得出x与y的和一定等于m的结论 |
|
| B. | 可以根据原子守恒,得出x与m的数值一定相等的结论 |
|
| C. | 可以根据氧化还原反应中电子得失守恒,得出x的值等于4的结论 |
|
| D. | 可以根据氧化还原反应中各种关系,得出R2+是还原剂,O2是氧化剂,R3+是氧化产物,H2O是还原产物的结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:
向100mL的FeBr2溶液中通入标准状况下Cl25.04L,Cl2全部被还原,测得溶液中c(Br﹣)=c(Cl﹣),则原FeBr2溶液的物质的量浓度是( )
|
| A. | 0.75mol/L | B. | 1.5mol/L | C. | 2mol/L | D. | 3mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M.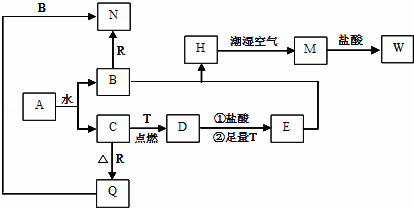
(1)写出下列物质的化学式:A: ,D: ,R: .
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式: ;B和R反应生成N的离子方程式: ;D与盐酸反应的离子方程式: .
(3)检验气体C的方法: .
查看答案和解析>>
科目:高中化学 来源: 题型:
由乙烯合成有机物F(二乙酸乙二酯),采用下列合成路线:
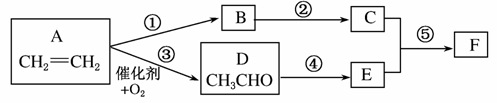
(1)已知有机物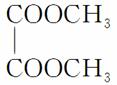 的名称为乙二酸二甲酯。请写出F的结构简式__________。
的名称为乙二酸二甲酯。请写出F的结构简式__________。
(2)在上述反应中属于取代反应的有________(填反应代号)。
(3)A、D、E、F中能引入C中官能团的物质有__________(填反应物代号),其反应⑤的化学方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应_________________,负极反应_________________。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:________________________________。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式_____________、_______________。
劣质不锈钢腐蚀的实验现象:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com