
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 全部 |
分析 勒夏特列原理:如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动. 勒夏特列原理是指在一个平衡体系中,若改变影响平衡的一个条件,平衡总是要向能够减弱这种改变的方向移动.比如一个可逆反应中,当增加反应物的浓度时,平衡要向正反应方向移动,平衡的移动使得增加的反应物浓度又会逐步减少;但这种减弱不可能消除增加反应物浓度对这种反应物本身的影响,与旧的平衡体系中这种反应物的浓度相比而言,还是增加了.
解答 解:①实验室常用饱和NaHCO3溶液除去CO2中混有的SO2气体,溶液中存在二氧化碳的溶解平衡,碳酸氢根降低了二氧化碳的溶解度,可以用勒夏特列原理解释,故正确;
②氯水在溶液中存在溶解平衡,长期放置、次氯酸分解,平衡正向移动,最终成为盐酸,可以用勒夏特列原理解释,故正确;
③催化剂只是影响反应速率,不能用勒夏特列原理解释,故错误;
④在重铬酸钾(K2 Cr2O7)水溶液中橙红色的Cr2O72-与黄色的CrO42-有以下平衡关系:Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq),故能够用勒夏特列原理解释,故正确;
⑤二氧化氮和四氧化二氮混合气体的密闭容器置于热水中,化学平衡向着生成二氧化氮的方向进行,颜色变深,能用勒夏特利原理解释,故正确;
⑥将装有Na2S2O3溶液与稀硫酸混合液的容器浸入热水中,发生氧化还原反应生成二氧化硫和单质硫,不能用勒夏特列原理解释,故B错误;
⑦在醋酸溶液中存在电离平衡,加入一些醋酸钠固体,抑制醋酸的电离,所以溶液的pH增大,能用勒夏特列原理解释,故正确;
能用勒夏特列原理解释的是:①②④⑤⑦;
故选B.
点评 本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃棒下端要靠在三层滤纸处 | |
| B. | 滤纸边缘低于漏斗边缘,多余部分要剪去,并用水润湿贴紧,不留气泡 | |
| C. | 过滤时将液体沿玻璃棒注入过滤器,并使液面高于滤纸边缘 | |
| D. | 漏斗下端紧靠烧杯内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
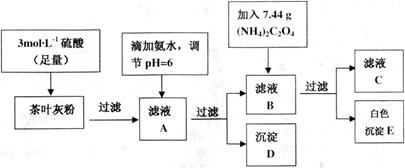
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
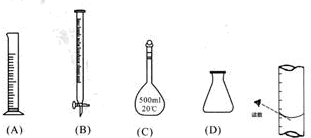
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑥⑦ | B. | ①②④⑤⑥ | C. | ⑤⑦ | D. | ④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液 | B. | 酚酞试液 | C. | 石蕊试液 | D. | 氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应. )与乙醇(
)与乙醇( )反应生成酯(
)反应生成酯( )和水的反应机理,反应过程中酸分子断裂C-O单键,醇分子断裂O-H键.试完成下列反应方程式:
)和水的反应机理,反应过程中酸分子断裂C-O单键,醇分子断裂O-H键.试完成下列反应方程式: +CH3CH2-18O-H$\stackrel{一定条件}{→}$CH3CO18OCH2CH3+H2O.
+CH3CH2-18O-H$\stackrel{一定条件}{→}$CH3CO18OCH2CH3+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com