
| 0.1mol×(7-2) |
| 2×(7-6) |
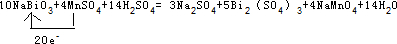 ,
,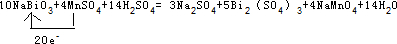 ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图中A、B、C、D是同周期或同主族的相邻元素:
如图中A、B、C、D是同周期或同主族的相邻元素:查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉和纤维素的最终水解产物都是葡萄糖,二者互为同分异构体 |
| B、石油经过分馏及裂化等工序得到的物质均为纯净物 |
| C、苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
D、结构片段 的高聚物,其单体是苯酚和甲醛 的高聚物,其单体是苯酚和甲醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ccl4 |
| 浓H2So4 |
| △ |
| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
| A、①② | B、③④ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B、利用蛋白质的颜色反应可以鉴别所有的蛋白质 |
| C、多糖、蛋白质、脂肪和聚丙烯等都属于高分子化合物 |
| D、食醋中的主要成分为乙酸,普通食醋中含有3%-5%的乙酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com