
| A�� | ��pH=6��H2SO4 ϡ��1000����c��H+��=2 c��SO42-�� | |
| B�� | 0.1 mol L-1�� Na2CO3��Һ�У�c��OH- ��=c��HCO3- ��+c��H+��+c��H2CO3�� | |
| C�� | Ũ�Ⱦ�Ϊ0.1 mol L-1�� NaClO ��Һ�� CH3COONa ��Һ�У�c��ClO-����c��CH3COO-�� | |
| D�� | Ũ�ȷֱ�Ϊ0.1 mol L-1��0.01 mol L-1��CH3COOH��Һ�У�c��CH3COO-��ǰ���Ǻ��ߵ�10�� |
���� A��ϡ��������������ʵ������䣬��ʱ��Ҫ����ˮ�ĵ��룻
B��������Һ�������غ������
C��ˮ��̶�Խ����Һ������Ũ��ԽС������������ӵ�ˮ��̶ȴ��ڴ�������ӣ�
D������Ϊ���ᣬ����Ũ��ԽС�������̶�Խ��
��� �⣺A��ϡ��������������ʵ������䣬����Һ�ӽ�����ʱҪ����ˮ�ĵ��룬���Խ�pH=6��������Һϡ��1000����c��SO42-��=$\frac{1}{2}$��10-9mol/L��c��H+��=10-7mol/L����Һ�е�SO42-��H+Ũ�ȵı�ֵԼΪ1��200����A����
B.1.0mol/L Na2CO3��Һ�д��������غ㣺c��OH-��=c��HCO3-��+c��H+��+2c��H2CO3������B����
C������������ӵ�ˮ��̶ȱȴ�������ӵ�ˮ��̶ȴ����c��ClO-����c��CH3COO-������C��ȷ��
D��Ũ�ȷֱ�Ϊ0.1 mol L-1��0.01 mol L-1��CH3COOH��Һ�У���Ϊ�������������˵��Ũ��ԽС������̶�Խ����������Һ�е����µĹ�ϵ��c��CH3COO-��ǰ��С�ں��ߵ�10������D����
��ѡC��
���� ���⿼��������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ���ȷ�ε�ˮ��ԭ������Ӱ��Ϊ���ؼ���ע�����յ���غ㡢�����غ㼰�����غ�ĺ��弰Ӧ�÷���������������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2mol/L MgCl2��Һ | B�� | 2.5mol/L NaCl��Һ | ||
| C�� | 1mol/L AlCl3��Һ | D�� | 5mol/L KClO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
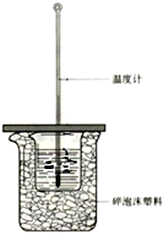 50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ����ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ�
50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ����ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{{K}_{W}}{C��{H}^{+}��}$=0.1mol/L����Һ�У�K+��Fe2+��Cl?��NO-3 | |
| B�� | ˮ�����H+Ũ��Ϊ1��10-12 mol/L����Һ��K+��Ba2+��Cl-��Br- | |
| C�� | ����NH4HCO3����������ݵ���Һ�У�Na+��Mg2+��ClO-��S2- | |
| D�� | �ӽ������ܲ�����������Һ�У�Ca2+��NH4+��Cl-��HSO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn��s��+CuSO4��aq���TZnSO4��aq��+Cu��s����H=-216 kJ•mol-1����Ӧ���������������������� | |
| B�� | ��ͬ�����£����1 mol��ԭ�������е�����ΪE1��1 mol����������е�����ΪE2����2E1=E2 | |
| C�� | 101 kPaʱ��2H2��g��+O2��g���T2H2O��l����H=-571.6 kJ•mol-1����H2��ȼ����Ϊ571.6 kJ•mol-1 | |
| D�� | H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����1 mol NaOH���������ƹ����뺬0.5 mol H2SO4��ϡ�����Ϻ�ų�57.3 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �Ȼ�������Һ��ͨ��������2Fe2++Cl2�T2Fe3++2Cl- | |
| B�� | ̼������ڴ��CaCO3+2H+�TCa2++CO2��+H2O | |
| C�� | �Ȼ�����Һ�м��������ˮ��Al3++4NH3•H2O�TAlO2-+4NH4++2H2O | |
| D�� | ����ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+HCO3-�TCaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
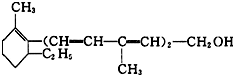
| A�� | ά����A�ķ���ʽΪC16H25O | B�� | ά����A��һ����������3��˫�� | ||
| C�� | ά����A���б����ṹ | D�� | ά����A�ķ����к������ֹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Al2O3 | B�� | H2SO3 | C�� | H2S | D�� | NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������������� | |
| B�� | ClO2��������ˮ���� | |
| C�� | ˮ�������ݹ���ľ�ļ��ܷ��������ͻ� | |
| D�� | Si����������ά |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com