
【题目】下列氧化还原反应中,水既不做氧化剂又不做还原剂的是( )
A. CaO + H2O===Ca(OH)2 B. C+H2O(g)![]() CO+H2
CO+H2
C. 2F2 + 2H2O===4HF + O2 D. 2Na2O2 +2H2O===4NaOH + O2 ↑
【答案】D
【解析】
有元素化合价变化的反应为氧化还原反应,水中H、O元素的化合价都没有变化时水既不做氧化剂又不做还原剂,以此来解答。
A. 反应前后,Ca、H、O各元素的化合价均不变,不属于氧化还原反应,故A错误;
B.碳元素化合价由0价升高到+2价,碳作还原剂;水中的氢元素化合价由+1价降低到0价,水作氧化剂,故B错误;
C. 氟元素由0价降低到-1价,做氧化剂;水中的氧元素由-2价升高到0价,做还原剂,故C错误;
D. 过氧化钠中O元素的化合价即升高到0价,又降低到-2价,属于氧化还原反应,且水中H、O元素的化合价不变,则水既不作氧化剂又不作还原剂,故D正确;
综上所述,本题选D。


 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案科目:高中化学 来源: 题型:
【题目】某铬铁矿主要成分是FeO·Cr2O3,含有FeCO3、SiO2、Fe3O4等杂质,现由该铬铁矿制备强氧化剂Na2Cr2O7的流程如下:
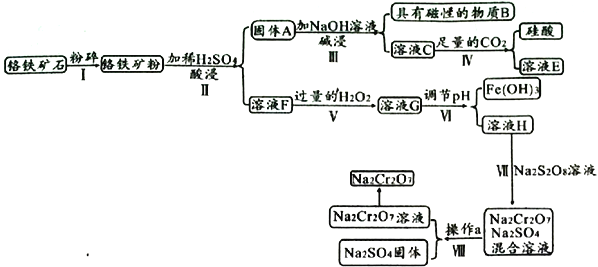
已知:常温下,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Cr(OH)3]=6.3×10-30
回答下列问题:
(1)物质B为______________,溶液E为____________________。
(2)溶液G中经检测不含H2O2的可能原因是________________________________________。
(3)若步骤Ⅵ调节pH后,c(Cr3+)=6.3mol/L,则pH范围是______________(离子浓度不大于1.0×10-5mol/L即可认为沉淀完全)。
(4)步骤Ⅶ发生的离子方程式为________________________________________。
(5)Na2Cr2O7和Na2SO4的溶解度随温度变化的曲线如下图所示,步骤Ⅷ中操作a为___________、__________________。
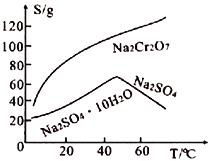
(6)若称取mg该铬铁矿,其中FeO·Cr2O3的质量分数为70%,最终制得ng Na2Cr2O7固体,则该过程中Cr元素的转化率为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2:326.26.26 联合国将2011年定为“国际化学年”,主题是“化学,人类的生活,人类的未来”,以鼓励青年人热爱化学。学习化学应该明白“从生活中来,到生活中去”的道理。

请填空:
(1)成人每天应从食物中摄取的几种元素的质量分别为: Mg 300 mg、Ca 800 mg、Fe 14 mg、Cu 1.6 mg,这些元素的物质的量之比为_________。
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式C6H12O6)的水溶液,其标签上的部分内容如右图所示。利用标签所提供的信息,计算出该注射液中葡萄糖的物质的量浓度为__________。
(3)SO2有毒,但葡萄酒里都含有微量SO2,起保鲜、杀菌和抗氧化作用,抗氧化作用利用了SO2的_______性。“硅胶”常用作实验室和袋装食品、瓶装药品等的干燥剂,也可以用作_______的载体。实验室可用________溶液来鉴别某未知液是苏打水还是水玻璃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中,有下列反应发生: ①N2 + O2 = 2NO;②2NO+O2=2NO2;③3NO2 + H2O = 2HNO3 + NO;④ 2SO2+O2 = 2SO3;⑤ SO3 + H2O = H2SO4; ⑥SO2+H2O![]() H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下MnO2氧化浓HCl的反应方程式如下:
(1)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,则MnO2、Cl2的氧化性由强到弱的顺序是:______________________。
MnCl2+Cl2↑+2H2O,则MnO2、Cl2的氧化性由强到弱的顺序是:______________________。
(2)用“双线桥法”标明反应中电子转移的方向和数目_______________________
(3)浓盐酸在反应中显示出来的性质是________(填编号)
A只有还原性 B还原性和酸性 C只有氧化性 D氧化性和酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
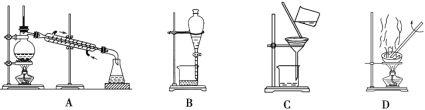
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl等杂质,选择装置________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________(填“上”或“下”)口进水。装置B在操作时为使液体顺利滴下,除打开下端活塞外,还应进行的具体操作是________________________________。
(4)为了除去KCl中的Ca2+、Mg2+、![]() 及泥沙,得到纯净的KCl,可将混合物溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序进行提纯,正确的步骤及顺序是___________。
及泥沙,得到纯净的KCl,可将混合物溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序进行提纯,正确的步骤及顺序是___________。
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液 ⑥加过量KOH溶液 ⑦加过量K2CO3溶液
A.②⑤④①③ B.⑥⑤⑦①③ C.④①②⑤③ D.④②⑤①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2HI+Cl2=2HCl+I2,②2Fe+3Cl2=2FeCl3,③2FeBr2+3Cl2=2FeCl3+2Br2.在一定条件下HI、Fe、FeBr2分别与足量的Cl2反应,如果三个反应电子转移数目相等,则HI、Fe、FeBr2的物质的量之比为
A. 1:1:1 B. 1:3:3 C. 3:1:1 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2 mol氢气完全燃烧生成水蒸气时放出能量484 kJ,且氢气中1 mol H—H键完全断裂时吸收能量436 kJ,水蒸气中1 mol H—O键形成时放出能量463 kJ,则氧气中1 mol O=O键断裂时吸收能量为( )
A. 920 kJ B. 557 kJ C. 496 kJ D. 188 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com