
【题目】下列说法正确的是
A. 某试样焰色反应呈黄色,则试样中肯定不含有K+
B. 过滤操作时,为了加快过滤可以用玻璃棒搅拌漏斗的液体
C. 蒸馏装置中,温度计水银球的位置应该在蒸馏烧瓶的支管口附近
D. 粗盐的提纯实验中,滤液在坩埚中加热蒸发结晶
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中错误的是( )
A. 构成原电池的正极和负极必须是两种不同的金属
B. 原电池是将化学能转变为电能的装置
C. 在原电池中,电子流出的一极是负极,发生氧化反应
D. 原电池放电时,电流的方向是从正极到负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是( )
A. 煅烧石灰石制生石灰B. 灼热的碳与水蒸气反应
C. 湿法炼铜(Fe+CuSO4)D. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol燃料完全燃烧的数据分别为:
燃料 | 一氧化碳 | 甲烷 | 异辛烷(C8H18) | 乙醇 |
△H | ﹣283.0kJmol﹣1 | ﹣891.0kJmol﹣1 | ﹣5461.0kJmol﹣1 | ﹣1366.8kJmol﹣1 |
使用上述燃料.最能体现“低碳经济”理念的是( )
A.一氧化碳
B.甲烷
C.异辛烷
D.乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( ) 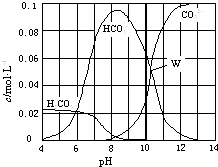
A.W点所示的溶液中:c(CO32﹣)=c(HCO3﹣)>c(OH﹣)>c(H+)
B.pH=4的溶液中:c(H2CO3)+c(HCO3﹣)+c(CO32﹣)=0.1molL﹣1
C.pH=8的溶液中:c(Na+)>c(HCO3﹣)>c(H2CO3)>c(CO32﹣)
D.pH=11的溶液中:c(Na+)+c (H+)=c(OH﹣)+c(Cl﹣)+c(CO32﹣)+c(HCO3﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面均是正丁烷与氧气反应的热化学方程式(25℃、101kPa):
①C4H10(g)+ ![]() O2(g)═4CO2(g)+5H2O(l);△H=﹣2 878kJmol﹣1
O2(g)═4CO2(g)+5H2O(l);△H=﹣2 878kJmol﹣1
②C4H10(g)+ ![]() O2(g)═4CO2(g)+5H2O(g);△H=﹣2 658kJmol﹣1
O2(g)═4CO2(g)+5H2O(g);△H=﹣2 658kJmol﹣1
③C4H10(g)+ ![]() O2(g)═4CO(g)+5H2O(l);△H=﹣1 746kJmol﹣1
O2(g)═4CO(g)+5H2O(l);△H=﹣1 746kJmol﹣1
④C4H10(g)+ ![]() O2(g)═4CO(g)+5H2O(g);△H=﹣1 526kJmol﹣1
O2(g)═4CO(g)+5H2O(g);△H=﹣1 526kJmol﹣1
由此判断,正丁烷的燃烧热为( )
A.﹣2878 kJ/mol
B.﹣2 658kJ/mol
C.﹣1746 kJ/mol
D.﹣1526 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有如下反应:
①![]() +Cl2=Br2+
+Cl2=Br2+![]() ,②
,②![]() +5Cl-+6H+=3Cl2+3H2O,
+5Cl-+6H+=3Cl2+3H2O,
③2FeCl3+2KI=2FeCl2+2KCl+I2,④2FeCl2+Cl2=2FeCl3。
下列各微粒氧化能力由强到弱的顺序正确的是( )
A. ![]() >
>![]() >Cl2>Fe3+>I2 B.
>Cl2>Fe3+>I2 B. ![]() >Cl2>
>Cl2>![]() >I2>Fe3+
>I2>Fe3+
C. ![]() >
>![]() >Cl2>Fe3+>I2 D.
>Cl2>Fe3+>I2 D. ![]() >
>![]() >Fe3+>Cl2>I2
>Fe3+>Cl2>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用NaClO3与Na2SO3制取ClO2气体,再由ClO2在强碱性条件下与过量的H2O2反应制得漂白剂NaClO2(装置如图1所示). 
已知(如图2):(I)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO33H2O,高于38℃时析出晶体是NaClO2;(Ⅱ)30% H2O2超过40℃时会完全分解;(Ⅲ)高于60℃时NaClO2分解成NaClO3和NaCl.
(1)图1装置A发生的反应中,还原剂是 .
(2)图1装置B中反应生成NaClO2的化学方程式为 . ②实验中图1装置B需进行温度控制不超过40℃,在不改变NaOH溶液浓度和体积的条件下,可采取的措施有、 .
(3)请补充从图1装置B反应后的溶液中获得NaClO2晶体的操作步骤. ①在55℃ 时蒸发结晶;②;③;④;得到成品.
(4)图1装置C的作用是 .
(5)证明实验后图1装置B所得混合溶液中的NaClO2具有氧化性的实验方案是 . (可供选用的试剂:稀H2SO4、FeCl2溶液、KSCN溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,类比Mg与CO2反应的思路对Mg与NO2的反应进行预测并探究Mg与NO2的反应及产物. 
请回答下列问题:
(1)利用如图装置完成实验,连接的顺序为 (c)﹣﹣﹣(e)﹣(f)﹣﹣﹣﹣﹣ .
(2)装置A中盛装的干燥剂可以是(填序号). ①浓硫酸 ②无水CaCl2③碱石灰 ④五氧化二磷
(3)装置E的作用是(用化学方程式表示),装置B中盛放浓硝酸的仪器名称是 , 装置F的作用是 .
(4)为防止空气干扰实验,排净装置中空气的具体实验操作为 .
(5)已知装置D中初始加入的镁粉的质量为13.2g,在足量的NO2中充分燃烧,实验结束后,硬质玻璃管冷却至室温,称量,测得剩余固体的质量为21.0g,产生的气体体积为1120mL(标准状况),写出玻璃管中发生反应的化学方程式 .
(6)在设计上若没有干燥管是否可行?请解释原因 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com