
| A. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| B. | 12g金刚石中含有的C-C键的个数为2NA | |
| C. | 配位数为4的配合物均为正四面体结构 | |
| D. | 向含有0.1mol[Co(NH3)4Cl2]Cl的水溶液中加入足量AgNO3溶液只能生成0.1molAgCl |
分析 A.NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键,[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键;
B.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×$\frac{1}{2}$=2个C-C键;
C.配位数为4的配合物可以为正四面体结构,也可以为平面四边形结构,据此判断;
D.在配合物[Co(NH3)4Cl2]Cl中,有两个氯离子中内界,有一个氯离子在外界,溶液中能与银离子反应生成沉淀的是在外界的氯离子,由此可推断生成氯化银沉淀的物质的量.
解答 解:A.NH4+中氮原子提供孤电子对,氢原子提供空轨道,从而形成配位键,[Cu(NH3)4]2+中铜原子提供空轨道,氮原子提供孤电子对,所以形成配位键,故A正确;B.每个C原子与其他4个C原子共用4个C-C键,相当于每个C原子占有4×$\frac{1}{2}$=2个C-C键,1mol金刚石含2molC-C键,故B正确;
C.配位数为4的配合物可能为平面结构,如[Cu(NH3)4]2+为平面正方形结构,故C错误;
D.Ag++Cl-=AgCl↓,0.1mol[Co(NH3)4Cl2]Cl电离产生0.1mol氯离子,加入足量的AgNO3溶液,生成氯化银沉的物质的量是0.1mol,内界氯离子未沉淀,故D正确;
故选C.
点评 本题考查了配合物、金刚石的结构等知识,注意金刚石中含有C-C键的个数,注意配体和外界离子的区别,题目难度中等.


科目:高中化学 来源: 题型:推断题
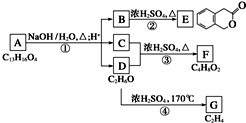 图中A、B、C、D、E、F、G均为有机化合物.根据下图回答问题.
图中A、B、C、D、E、F、G均为有机化合物.根据下图回答问题. .反应①的反应类型是水解反应(取代反应).
.反应①的反应类型是水解反应(取代反应).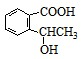 、
、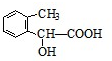 、
、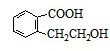 .
. 或CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH.
或CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
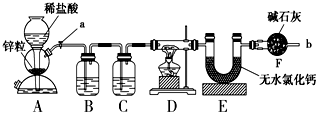
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中混有溴,加入KI溶液,振荡,用直馏汽油萃取,分液 | |
| B. | 硝基苯中混有浓硝酸,加入足量稀NaOH溶液洗涤,振荡,用分液漏斗分液 | |
| C. | 乙烯中含有SO2,将其通入装有KMnO4溶液的洗气瓶中进行洗气 | |
| D. | 乙烷中含有乙烯,通入适量的H2在一定条件下反应使乙烯转变成乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
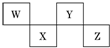
| A. | W、Y可形成两种不同的化合物 | |
| B. | Z的阴离子电子层结构与氩原子的相同 | |
| C. | W的简单氢化物的沸点比Y的氢化物的沸点高 | |
| D. | Y元素的非金属性比W元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
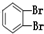
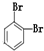 ⑪
⑪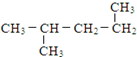 ⑫
⑫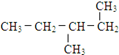
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加AgNO3溶液,观察是否有白色沉淀 | |
| B. | 滴加AgNO3溶液、稀硝酸和NaNO2溶液,观察是否有白色沉淀 | |
| C. | 滴加NaOH溶液,并加热片刻,再用稀硝酸酸化后,滴入AgNO3溶液观察是否有白色沉 | |
| D. | 滴加AgNO3溶液和稀硝酸,观察是否有白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有泥沙的浑水,静置一会儿水沙分离,可取得上层的清水 | |
| B. | 农村“扬谷”分离饱满的谷粒和干瘪的谷壳 | |
| C. | 建筑工地上用铁筛把大小不同的沙粒分开 | |
| D. | 淘米除去米中混有的小沙粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
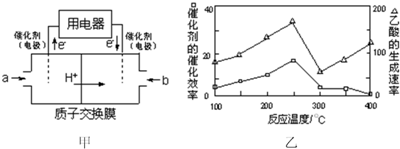
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com