
| 物 质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 乙 醇 | -114 | 78 | 0.789 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |

分析 (1)在浓硫酸作催化剂、加热条件下,乙酸和乙醇发生酯化反应生成乙酸乙酯;浓硫酸具有吸水性和催化能力;
(2)乙酸乙酯是难溶于碳酸钠溶液的无色液体,碳酸钠溶液呈碱性,酚酞遇碱变红色,所以碳酸钠溶液呈红色,生成的乙酸乙酯中含有乙醇和乙酸,乙醇极易溶于水,乙酸和碳酸钠反应生成乙酸钠、二氧化碳和水,导致溶液碱性降低;
(3)分离互不相溶的液体采用分液方法,分液所用的仪器是分液漏斗;
(4)甲、乙的区别是乙装置能冷凝回流.
解答 解:(1)在浓硫酸作催化剂、加热条件下,乙酸和乙醇发生酯化反应生成乙酸乙酯,反应方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;浓硫酸具有吸水性和催化能力,所以该反应中浓硫酸作催化剂和吸水剂,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;催化剂、吸水剂;
(2)乙酸乙酯是难溶于碳酸钠溶液的无色液体,碳酸钠溶液呈碱性,酚酞遇碱变红色,所以碳酸钠溶液呈红色,生成的乙酸乙酯中含有乙醇和乙酸,乙醇极易溶于水,乙酸和碳酸钠反应生成乙酸钠、二氧化碳和水,导致溶液碱性降低,所以看到的现象是在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄,
故答案为:在浅红色Na2CO3溶液上层有约4cm厚的无色液体,振荡后Na2CO3溶液层红色变浅,有气泡,上层液体变薄;上层是油层因为生成的乙酸乙酯难溶于水,且密度比水小,同时因为挥发出来的乙酸与碳酸钠反应,放出CO2气体,所以有气泡出现;
(3)分离互不相溶的液体采用分液方法,分液所用的仪器是分液漏斗,
故答案为:分液漏斗;上;乙酸乙酯比水密度小;
(4)甲、乙的区别是乙装置能冷凝回流,提高产率,所以选乙,
故答案为:乙,反应物能冷凝回流.
点评 本题考查物质制备,为高频考点,明确实验步骤及实验原理是解本题关键,侧重考查实验操作、实验分析能力,知道碳酸钠溶液作用,易错点是(4)题,题目难度不大.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | OH- | C. | Ag+ | D. | CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g/mol | B. | 32g/mol | C. | 64g/mol | D. | 128g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO${\;}_{4}^{2-}$ | B. | CO${\;}_{3}^{2-}$ | C. | OH- | D. | NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+、Al3+、Cl-、NO3- | B. | Fe2+、Na+、NO3-、SO42- | ||
| C. | Ba2+、Na+、K+、NO3- | D. | K+、Ca2+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
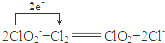 .
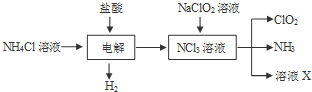
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的平均反应速率为0.15mol/(L•min) | |
| B. | 平衡时,A的转化率为20% | |
| C. | 平衡时,C的浓度为0.25mol/L | |
| D. | 容器内的起始压强和平衡压强之比为11:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4mol•L-1 | B. | 0.43mol•L-1 | C. | 0.8mol•L-1 | D. | 1.2mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com