
【题目】已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)常温下,浓度均为0.1molL﹣1的下列六种溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
①上述盐溶液中的阴离子,结合质子能力最强的是
②根据表中数据判断,浓度均为0.01molL﹣1的下列五种物质的溶液中,酸性最强的是;(填编号,下同)将各溶液分别稀释100倍,pH变化最小的是
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa═Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为
(2)CaCO3是一种难溶物质,其KSp=2.8×10﹣9 . 现将浓度为2×10﹣4 mol/L Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为 mol/L.
【答案】
(1)CO32﹣;D;C;CD;2Cl2+CO32﹣+H2O=CO2↑+2Cl﹣+2HClO
(2)5.6×10﹣5
【解析】解:(1)弱酸根质量水解程度越大,相同浓度的钠盐溶液的pH越大,则酸根离子结合质子能力越大,根据溶液pH知,CO32﹣的水解程度最大,则CO32﹣结合质子能力最强,所以答案是:CO32﹣;
①弱酸根质量水解程度越大,相同浓度的钠盐溶液的pH越大,则酸根离子结合质子能力越大,根据溶液pH知,CO32﹣的水解程度最大,则CO32﹣结合质子能力最强,所以答案是:CO32﹣;②酸的酸性越强,酸的电离程度越大,其酸根离子水解程度越小,相同浓度的钠盐溶液的pH越小,根据表中数据知,酸性最强的酸是CH3COOH、酸性最弱的酸是C6H5OH;加水稀释促进弱酸电离,相同浓度的不同酸稀释相同的倍数,酸的酸性越弱,酸的PH变化越小,酸性最弱的酸是C6H5OH,则pH变化最小的是C6H5OH,
所以答案是:D;C;③据各种酸对应钠盐的pH可知,其酸性醋酸的酸性比碳酸强,醋酸的酸性比HCN强,碳酸的酸性比HClO强,碳酸的酸性比苯酚强,苯酚的酸性比HCO3﹣强,所以CO2+H2O+NaClO═NaHCO3+HClO和CO2+H2O+C6H5ONa═NaHCO3+C6H5OH,所以CD错误,所以答案是:CD;④HClO和碳酸钠不反应,盐酸和碳酸钠反应生成二氧化碳,所以导致氯水中HClO浓度增大,离子方程式为2Cl2+CO32﹣+H2O=CO2↑+2Cl﹣+2HClO,
所以答案是:2Cl2+CO32﹣+H2O=CO2↑+2Cl﹣+2HClO;(2)等体积混合后溶液中碳酸根的浓度为2×l0﹣4mol/L÷2=1×l0﹣4mol/L,要生成CaCO3沉淀需要钙离子浓度为 ![]() mol/L=2.8×l0﹣5mol/L,故需要CaCl2溶液的最小浓度为2.8×l0﹣5mol/L×2=5.6×l0﹣5mol/L,
mol/L=2.8×l0﹣5mol/L,故需要CaCl2溶液的最小浓度为2.8×l0﹣5mol/L×2=5.6×l0﹣5mol/L,
所以答案是:5.6×10﹣5 .
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】为了研究土壤的酸碱性,某学生做了如下实验:将一定体积的蒸馏水加入一定质量的土壤中,充分搅拌后,过滤并留取滤液,测滤液的pH后向滤液中滴加氨水,每加入2mL氨水就搅拌均匀并测量溶液的pH,所得实验记录如下:
加氨水体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液的pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
利用上述记录的数据,以加入的氨水体积为横坐标、pH为纵坐标绘制曲线图,并根据曲线图回答下列问题:
(1)所测土壤的酸碱性如何?
(2)所用氨水的pH和c(OH﹣)分别为多少?
(3)为使该滤液呈中性,所加入氨水的恰当体积是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
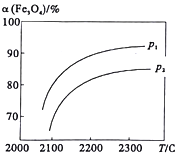
A. a>0
B. 压强p1>p2
C. 升高温度,该反应的平衡常数增大
D. 将体系中O2分离出去,能提高Fe3O4的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙醇在水中能电离出少量的H+,所以乙醇是电解质
B.乙醇与O2发生不完全燃烧生成乙醛
C.乙醇分子中所有的氢原子都可被钠置换出来
D.乙醇是一种很好的溶剂,能溶解多种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分 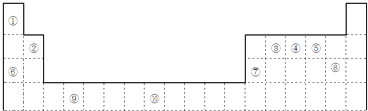
(1)元素⑩的次外层电子数为个.
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.写出元素②的氢氧化物与NaOH溶液反应的离子方程式;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJmol﹣1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是 . (填元素代号)
②T元素最可能是(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法错误的是( )
硫酸化学纯(CP)
(500mL)
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84g/cm3
质量分数:98%
A. 该硫酸试剂的物质的量浓度为18.4mol·L-1
B. 该硫酸与等体积的水混合所得溶液的质量分数大于49%
C. 配制200mL 4.6mol·L-1的稀硫酸需取该硫酸62.5mL
D. 常温下,将2.7gAl投入足量该硫酸中可得到标准状况下的氢气3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于浓硝酸和浓硫酸的叙述中正确的是
A.常温下都不可用铝制容器贮存
B.露置在空气中,容器内酸液的质量都减轻
C.常温下都能与铜较快反应
D.露置在空气中,容器内酸液的浓度都降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 单位体积溶液里所含的溶质的物质的量,叫做物质的量浓度
B. 气体摩尔体积就是22.4 L /mol
C. 摩尔质量就是微粒的相对分子质量或者相对原子质量
D. 物质的量就是物质的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com