
 如图是三种稀酸对FeCr合金随Cr含量变化的腐蚀性实验结果,
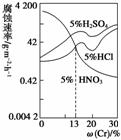
如图是三种稀酸对FeCr合金随Cr含量变化的腐蚀性实验结果,
下列有关说法正确的是 ( )
A.稀硝酸对FeCr合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是Fe+6HNO3(稀)===Fe(NO3)3
+3NO2↑+3H2O
C.Cr含量大于13%时,因为三种酸中硫酸的氢离子浓度最大,
所以对FeCr合金的腐蚀性最强
D.随着Cr含量增加,稀硝酸对FeCr合金的腐蚀性减弱
科目:高中化学 来源: 题型:
元素周期表中某区域的一些元素多用于制造半导体材料,它们是 ( )
A.左、下方区域的金属元素 B.右、上方区域的非金属元素
C.过渡元素中 D.金属元素与非金属元素分界线附近的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是 ( )
A.工业上电解熔融状态的Al2O3制备Al涉及氧化还原反应 (2012·广东理综,10B)
B.四川灾区重建使用了大量钢材,钢材是合金 (2009·广东,5②)
C.金属材料都是导体,非金属材料都是绝缘体 (2008·山东理综,9A)
D.合金材料中可能含有非金属元素 (2009·山东理综,9A)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列制备金属单质的方法或原理正确的是 ( )
A.在高温条件下,用H2还原MgO制备单质Mg
B.在通电条件下,电解熔融Al2O3制备单质Al
C.在通电条件下,电解饱和食盐水制备单质Na
D.加强热,使CuO在高温条件下分解制备单质Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究。查阅相关资料后,猜想该绿色物质可能是铜的碳酸 盐。
盐。
该小组同学利用下图装置进行实验(部分夹持仪器略)。
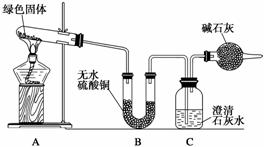
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。
观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是______________________________________________。
(2)加热后试管中剩余的黑色物质是________________________________________。
(3)假设该绿色物质是一种纯净物,则其化学式可能是________________________,加热分解的化学方程式为________________________________________________________
__________________________________________ ______________________________。
______________________________。
(4)上述实验步骤③中的反应的离子方程式为__________________________________
________________________________________________________________________。
(5)实验装置最后的干燥管的作用是_________________________________________。
(6)如果将B、C两装置对调,能否达到实验目的________(填“能”或“不能”),为什么?________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,水的电离达到平衡:H2OH++OH-。下列叙述正确的是( )
A.将水加热,平衡向正反应方向移动,KW不变
B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大
C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低
D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期中的A、B、C、D、E五种元素,原子序数依次增大。A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,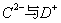 的核外电子数相等。则下列说法正确的是
的核外电子数相等。则下列说法正确的是
A.B与A只能组成BA3化合物
B.C、D、E形成的化合物水溶液可能显碱性
C.A、B、C形成的化合物一定不能发生水解反应
D.E的氧化物对应的水化物只具有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
已知空气—锌电池的电极反应为:锌片:Zn+2OH--2e- = ZnO+H2O;
碳棒:1/2 O2+H2O+2e- = 2OH-,据此判断,锌片是
A.正极,并被还原 B.正极,并被氧化 C.负极,并被还原 D.负极,并被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com