
| A. | NaCl | B. | FeSO4 | C. | K2CO3 | D. | NH4Cl |
分析 水的电离方程式为H2O?H++OH-,加入的物质或离子能影响水电离平衡的移动,则破坏水的电离.
解答 解:A、氯化钠电离出的钠离子和氯离子均不能与水电离出的氢离子和氢氧根离子结合,不影响水的电离,故A选;
B、硫酸亚铁电离出的亚铁离子结合水电离出的氢氧根,破坏水的电离平衡,故B不选;
C、碳酸钾电离出的碳酸根结合水电离出的氢离子,破坏水的电离平衡,故C不选;
D、氯化铵电离出的铵根结合水电离出的氢氧根离子,破坏水的电离平衡,故D不选,故选A.
点评 本题考查了水的电离,酸或碱能抑制水的电离,含有弱根离子的盐能促进水的电离,根据溶液中氢离子和氢氧根离子浓度是否变化来确定是否破坏水的电离.


科目:高中化学 来源: 题型:选择题
| A. | 用燃烧的方法可以鉴别甲烷和乙烯 | |
| B. | 用酸性KMnO4溶液鉴别苯和CCl4 | |
| C. | 用银氨溶液鉴别蔗糖和葡萄糖 | |
| D. | 用KI溶液鉴别淀粉溶液和鸡蛋白溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol苯分子中含有C=C双键数目为1.5 NA | |
| B. | 常温常压下,17 g 羟基含有的电子总数为9NA | |
| C. | 标准状况下,11.2 L CHCl3 中含有的共价键数目为2NA | |
| D. | 将1 mol蔗糖与稀H2SO4混合使之完全水解,可生成2NA个葡萄糖分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑩ | |
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式和结构都相同,性质可能相同 | |
| B. | 分子式相同,结构不同,化学性质一定不相同 | |
| C. | 相对分子质量一定相同、官能团一定不同 | |
| D. | 相对分子质量和各元素质量分数一定相同,化学性质不一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子的核素符号:14C | B. | HF的电子式: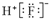 | ||
| C. | Cl-离子的结构示意图: | D. | 氧化铝的化学式:AlO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com