
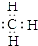 ;②Cl-的结构示意图:
;②Cl-的结构示意图: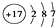 ;③乙烯的分子式:CH2=CH2④中子数为20的氳原子:${\;}_{17}^{37}$Cl;⑤乙酸分子的比例模型:
;③乙烯的分子式:CH2=CH2④中子数为20的氳原子:${\;}_{17}^{37}$Cl;⑤乙酸分子的比例模型: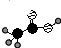 ;⑥氯乙烷的结构式:
;⑥氯乙烷的结构式: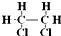
| A. | ④ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ①③④⑤⑥ |
分析 ①甲基中含有3个碳氢键,碳原子最外层为7个电子;
②氯离子质子数为17,有3个电子层,最外层有8个电子;
③乙烯的结构简式中没有标出官能团碳碳双键;
④中子数为20的氯原子,质量数为17+20=37;
⑤比例模型是原子紧密连起的,只能反映原子大小,大致的排列方式与空间构型;
⑥氯乙烷中含有1个氯原子.
解答 解:①甲基中碳原子最外层为7个电子,甲基的电子式为 ,故错误;
,故错误;
②氯离子质子数为17,有3个电子层,最外层有8个电子,离子结构示意图为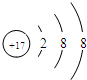 ,故错误;
,故错误;
③乙烯分子中含有碳碳双键,结构简式为CH2=CH2,故错误;
④中子数为20的氯原子,质量数为17+20=37,符号为:${\;}_{17}^{37}$Cl,故正确;
⑤乙酸的结构简式为 ,所以比例模型为
,所以比例模型为 ,故错误;
,故错误;
⑥氯乙烷的结构式: ,故错误;
,故错误;
故选A.
点评 本题考查了比例模型、电子式、结构式、结构简式的判断,题目难度中等,注意掌握常见的化学用语的概念及正确表示方法,试题培养了学生灵活应用所学知识的能力.


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

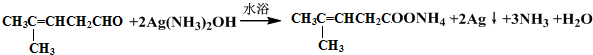
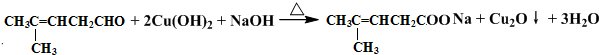 ;然后往反应后的溶液中加入稀硫酸至溶液呈酸性,再滴加足量的溴水,检验分子中碳碳双键,生成的有机产物的结构简式是
;然后往反应后的溶液中加入稀硫酸至溶液呈酸性,再滴加足量的溴水,检验分子中碳碳双键,生成的有机产物的结构简式是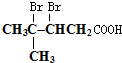 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中混有溴,加入KI 溶液,振荡,用 CCl4萃取出溴 | |
| B. | 乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 硝基苯中混有浓 HNO3 和浓 H2SO4,将其倒入到 NaOH 溶液中,静置,分液 | |
| D. | 乙烯中混有 SO2,将其通入酸性 KMnO4 溶液中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐、淡水 | B. | 氯、溴、碘 | C. | 钠、镁、铝 | D. | 烧碱、氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色 | |
| B. | 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色 | |
| C. | 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色 | |
| D. | 碘水,变蓝色; 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
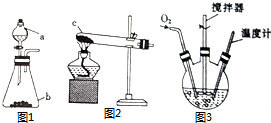 氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂.实验室可用废铜屑、浓盐酸、食盐及氧气制取CuCl.已知KMnO4不与稀盐酸反应,回答下列问题:
氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂.实验室可用废铜屑、浓盐酸、食盐及氧气制取CuCl.已知KMnO4不与稀盐酸反应,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com