
某气态烃A与H2的相对密度为14,其产量可以用来衡量一个国家的石油化工发展水平。以该化合物为原料合成化合物G、E和I的流程如下:
已知:Ⅰ.芳香族化合物F为C、H、O化合物,其相对分子质量为166,环上的一氯代物有一种,1 mol F与足量NaHCO3溶液反应能生成2 mol CO2,F与足量B反应生成G。
Ⅱ.H为二元醇,其蒸气密度折算成标准状况为2.77 g/L,H与足量D反应生成I。
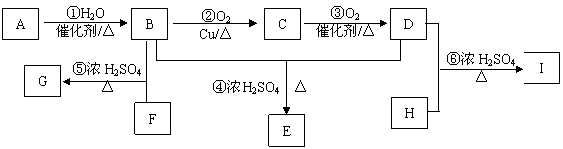
(1)A中官能团的名称为 ,E的结构简式 。
(2)G的分子式为 ,反应⑤的反应类型为 。
(3)写出下列化学方程式:
② ;
⑥ ;
(4)F与H可生成高分子化合物J,写出生成J的化学反应方程式:
。
(5)I有多种同分异构体,其中一类同分异构体有如下特征:
①分子中含有五元环结构;②1 mol该有机物与足量NaHCO3溶液反应,能生成1 mol CO2;③1 mol该有机物与足量Na反应,能生成1.5 mol H2;④环上的一氯代物只有三种。则满足以上条件的有机物的所有可能的结构简式为:
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.通过石油分馏可以获得大量的芳香烃
B.石油裂化的目的是为了得到乙烯、丙烯和苯
C.煤的干馏发生了化学变化
D.煤中含有苯和甲苯,可以通过先干馏后分馏的方法得到苯和甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
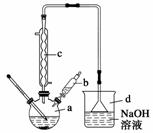
溴苯是一种常用的化工原料。实验室制备溴苯
的实验步骤如下:
步骤1:在a中加入15 mL苯和少量铁屑,再将b中4.0 mL
液溴慢慢加入到a中,充分反应。
步骤2:向a中加入10 mL水,然后过滤除去未反应的铁屑。高考资源网
步骤3:滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL 水洗涤,分液得粗溴苯。
 步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品。
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品。
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
(1)仪器d的作用是 。
(2)将b中的液溴慢慢加入到a中,而不能快速加入的原因是 。
(3)仪器c的作用是冷凝回流,回流的主要物质有 (填化学式)。
(4)步骤4得到的粗产品中还含有杂质苯。已知苯、溴苯的有关物理性质如上表,则要进一步提纯粗产品,还必须进行的实验操作名称是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素在周期表中位置的叙述正确的是
A.原子的最外层有2个电子的元素一定是ⅡA族元素
B.元素所在的主族序数与最外层电子数之比为1的元素都是金属元素
C.俄罗斯专家首次合成了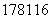 X原子,116号元素位于元素周期表中第七周期ⅥA族
X原子,116号元素位于元素周期表中第七周期ⅥA族
D.原子最外层电子数大于3(小于8)的元素一定是非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬酸的结构简式如图,下列说法正确的是
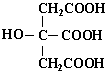 A.柠檬酸中能发生酯化反应的官能团有2种
A.柠檬酸中能发生酯化反应的官能团有2种
B.1 mol柠檬酸可与4 mol NaOH发生中和反应
C.1 mol柠檬酸与足量金属Na反应生成生成1.5 mol H2
D.柠檬酸与O2在Cu作催化剂,加热的条件下,能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl‾、S2‾、Ca2+、K+半径逐渐减小 D.35Cl2与37Cl2得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
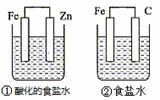 结合右图判断,下列叙述正确的是
结合右图判断,下列叙述正确的是
A.①和②中铁的腐蚀均被加速
B.①和②中负极反应均是Fe-2e-===Fe2+[来源:学科网]
C.②中碳棒上反应是O2+2H2O+4e-===4OH-
D.①装置中溶液pH会升高,②装置中溶液碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的化工原料。某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
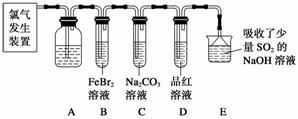
(1)实验室用二氧化锰和浓盐酸加热制取氯气,该反应的离子方程式为____________________________________________________________。
(2)装置A中盛有的试剂是饱和NaCl溶液,作用是_______________________________。
(3)若D中品红溶液褪色,则B装 置中发生反应的离子方程式是_____________________________________________________________。
置中发生反应的离子方程式是_____________________________________________________________。
某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气。经分析吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO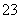 和SO
和SO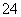 ,对于可能存
,对于可能存 在的其他阴离子,研究小组提出以下3种假设。
在的其他阴离子,研究小组提出以下3种假设。
假设1:只存在SO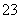 ; 假设2:只存在ClO-;假设3:既不存在
; 假设2:只存在ClO-;假设3:既不存在 SO
SO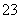 ,也不存在ClO-。
,也不存在ClO-。
(4)学习小组判断同时存在SO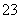 和ClO-是不可能的理由是_____________________。
和ClO-是不可能的理由是_____________________。
(5)现限选以下试剂,设计实验方案,进行实验,请写出实验步骤以及预期现象和结论。
a.3 mol·L-1 H2SO4 b.酸性KMnO4溶液 c.1 mol·L-1 BaCl2溶液
d.FeCl2溶液 e.酚酞试液
步骤一:取少量吸收液于试管中,滴加3 mol·L-1 H2SO4至溶液呈中性,然后将所得溶液分装于F、G两试管中。
步骤二:向F试管中滴加少量__________(填序号),若溶液____________________(填现象),则假设1成立。
步骤三:向G试管中滴加少量d溶液,生成红褐色沉淀,假设2成立,则反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe(OH)3胶体虽然是由FeCl3溶液制得,但两者是截然不同的两种物质。FeCl3溶液、Fe(OH)3胶体共同具备的性质是 ( )
A.都呈透明的红褐色
B.都比较稳定,密封保存一段时间都不会产生沉淀
C.分散质颗粒直径相同
D.当有光线透过时,都能产生丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com